Artículo científico
Recepción: 15 Abril 2020
Aprobación: 25 Mayo 2020
Resumen: El trabajo está basado en la degradación de fenol utilizando lodo rojo como un catalizador para procesos de oxidación avanzada solar (POA). Se aplicó un diseño de experimento factorial 23 con dos puntos al centro, la medición de la DQO se realizó mediante el Método HACH DR2010 y la concentración de fenol por el método 4-aminoantipirina. POA alcanzó degradaciones en la DQO del 94,1 % y de la concentración de fenol del 99,7 %. Se analizaron patrones secundarios para el HPLC, donde se garantizó la coincidencia espectral de los compuestos mediante una cromatografía de gases acoplada a masas (CG-MS). La identificación de las especies de la degradación de fenol se realizó a través de la Cromatografía líquida de alta resolución (HPLC) acoplado a un detector UV-HP DAD. La separación óptima de los patrones estudiados, fue con una fase móvil: agua/metanol (7:3), pH 4,0 ajustado con H3PO4 0,1 M, con un de flujo 0,5 mL/min, λ = 220 nm. Luego de obtenidas las condiciones de separación se identificaron en las muestras como productos de la degradación ácido oxálico, fórmico, acético e hidroquinona. Demostrando que el lodo rojo resultó apropiado para disminuir la concentración de la DQO y fenol mediante POA solar.
Palabras clave: lodo rojo, procesos de oxidación avanzada, GC-MS, HPLC, DQO.
Abstract: The work is based on the degradation of phenol using red mud as a catalyst for solar advanced oxidation processes (AOP). A factorial experiment design 23 was applied with two points at the center; the COD measurement was performed using the HACH DR2010 method and the phenol concentration by the 4-aminoantipyrine method. AOP achieved degradations in the COD of 94,1 % and of the phenol concentration of 99,7 %. Secondary standards were analyzed for HPLC, where the spectral coincidence of the compounds was guaranteed by mass coupled gas chromatography (CG-MS). The identification of the species of the phenol degradation was performed through High Performance Liquid Chromatography (HPLC) coupled to a UV-HP DAD detector. The optimal separation of the studied standards was with a mobile phase: water / methanol (7:3), pH 4,0 adjusted with 0,1 M H3PO4, with a flow of 0,5 mL/min, λ = 220 nm. After the separation conditions were obtained, the samples were identified as degradation products oxalic, formic, acetic acid and hydroquinone. Demonstrating that the red mud was appropriate to decrease the COD and phenol concentration by means of solar AOP.
Keywords: red mud, advanced oxidation processes, GC-MS, HPLC, CDO.
1. Introducción
El fenol es uno de los contaminantes ambientales más peligrosos y frecuentes en aguas residuales de las industrias químicas, petroquímicas, agroalimentarias y farmacéuticas, debido a su elevada toxicidad, bioacumulación, poca biodegradabilidad y a su carácter cancerígeno [1, 2, 3]. El fenol y sus derivados son considerados como residuos peligrosos debido a que son clasificados como compuestos orgánicos persistentes (COP) en aguas, donde los tratamientos biológicos proporcionados al agua residual (de mayor uso doméstico e industrial) no han mostrado ser efectivos al momento de la remoción, ya que los efluentes con estas características exhiben altos valores de Demanda Química de Oxígeno (DQO) y Demanda Biológica de Oxígeno (DBO) [4].
Para la degradación de estos COP se han utilizado diferentes métodos de tratamiento terciarios de aguas, tales como la nanofiltración, microfiltración, electrocoagulación, procesos de oxidación avanzada con hierro y lámparas UV, así como tratamientos combinados de fotocatálisis (TiO2) y oxidación electrolítica [5]. La aplicación de algunas de estas tecnologías ha resultado en la exitosa disminución de la concentración de fenol y sus derivados en los efluentes tratados. A pesar de los buenos resultados obtenidos al utilizar estas metodologías, se han determinado algunos inconvenientes en las mismas, por ejemplo, la utilización de catalizadores genera altos costos e inconvenientes de manejo, las técnicas de radiación artificial (lámparas UV) incrementan los costos motivado a la tecnología que requiere el montaje de éste tipo de plantas.
Los procesos de oxidación avanzada (POA) son una alternativa probada para el tratamiento de efluentes contaminados con fenol y sus derivados. Los POA pueden definirse como procesos de oxidación basados en la acción de especies altamente reactivas (radicales hidroxilos, •OH) que conducen a la degradación y mineralización de los compuestos contaminantes y a la inhibición de organismos patógenos [5, 6]. Los radicales al ser especies oxidantes energéticos, son capaces de oxidar compuestos orgánicos por abstracción de hidrógeno o por adición electrofílica al doble enlace, generándose radicales orgánicos libres (ecuaciones (1) y (2)).
 (1)
(1)
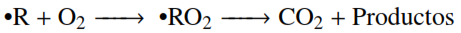 (2)
(2)Los lodos rojos tratados como catalizador en los POA, llevan a cabo dos técnicas de oxidación combinadas, como es el FotoFenton-like debido al contenido de hierro (Fe3+) y la fotocatálisis por la presencia de titanio (Ti) en los lodos rojos [7]. El proceso Foto-Fenton es una técnica particular de los POA, debido a que utilizan peróxido de hidrógeno (H2O2) para la formación de radicales libres en presencia de iones ferrosos (Fe2+), los cuales se oxidan a iones férricos (Fe3+) (ecuación (3)), en presencia de luz (hv). Al mismo tiempo la técnica FotoFenton-like utiliza la fotoreducción del Fe3+ a Fe2+ formando un acuocomplejo metal-carga-ligando (ecuación (4)) [7,8, 9].
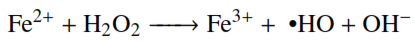 (3)
(3)
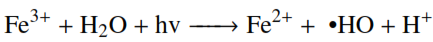 (4)
(4)Por otra parte la fotocatálisis hace referencia a una reacción catalítica que involucra la absorción de luz ultravioleta por parte de un catalizador, en específico el TiO2 realiza una óxido-reducción generando un par e– hueco y la consecutiva formación de radicales oxhidrilo y superóxido [10, 11, 12, 13, 14, 15].
Algunos investigadores tienen como propósito mejorar las potencialidades catalíticas del lodo rojo, con el fin de reducir controladamente los residuos del mismo, para producir sistemas activos con aplicaciones medioambientales [16], lograron producir sistemas de lodos rojos activos para aplicaciones ambientales diferentes, como son, oxidación avanzada mediante la reacción de Fenton heterogénea y la reducción de Cr (VI) en medio acuoso. La caracterización del catalizador mostró que a diferentes temperaturas de calcinación entre 300 y 600 °C, el H2 reduce el lodo rojo a diferentes fases, principalmente Fe3O4, FeO / Fe3O4 y FeO, siendo estas fases activas catalíticamente. La reducción con H2 a 400 °C mostró los mejores resultados para la oxidación del colorante azul de metileno como molécula modelo con condiciones de reacción con un H2O2 a pH neutro debido a la presencia del compuesto Fe0 / Fe+3 o Fe+4. Logrando por último regenerar el catalizador, para cerrar el ciclo ambiental. En éste orden de ideas es importante señalar que los lodos rojos, también han tenido aplicaciones como catalizadores heterogéneos en los procesos de oxidación avanzada tipo fotoquímico como el foto Fenton-like utilizando lámpara UV de mercurio de 400W como fuente de radiación. Según la investigación desarrollada por Galvickova y colaboradores [17] el lodo rojo puede convertirse en un eficiente catalizador para la eliminación de fenol en agua obteniendo resultados altamente eficaces. De igual manera se utilizó éste material activado por calcinación para la degradación fotocatalítica de Bisfenol A, obteniendo resultados de degradación entre 88 y 100 % utilizando una lámpara UV de 16W. Los estudios demuestran como la activación del lodo rojo mediante la calcinación y la neutralización con ácido, puede mejorar sus propiedades fisicoquímicas y también potenciar sus propiedades fotocatalíticas con el fin de incrementar su actividad en la fotodegradación de especies químicas contaminantes [18], evidenciándose un incremento del área superficial en un factor de 30 mediante la adición de HCl y un secado a 110 °C. Logrando una descomposición del Naranja de metilo mediante una lámpara UV en un 92,4 %. Evidenciando el uso reciente del lodo rojo como fotocatalizador heterogéneo de bajo costo en los procesos de oxidación avanzada.
Debido a la cantidad de variables que afectan las fotoreacciones durante el POA para el tratamiento de efluentes fenólicos, el diseño de experimentos (DDE) se emplea como una herramienta metodológica y estadística, que permite visualizar las posibles interacciones entre las variables estudiadas, verificando las correlaciones entre los parámetros analizados [19, 20, 21]. El presente estudio tiene como objetivo la identificación por HPLC de los productos generados de la fotodegradación del fenol mediante procesos de oxidación avanzados solar utilizando lodos rojos como catalizador.
2. Metodología
La investigación se desarrolló a través de un diseño de experimento tipo factorial 23 con dos puntos al centro teniendo como factores de entrada:
-
Cantidad de catalizador,
-
Cantidad de peróxido y
-
pH ajustado
y como variable de respuesta: la DQO, como se observa en la Tabla 1. La reacción de oxidación avanzada solar se llevó a cabo en un balón de tres bocas de volumen 250 mL (vidrio borosilicato), siguiendo la metodología propuesta por Ramos y colaboradores [22], Yamal y colaboradores [23]. Al reactor bach se le agregó un volumen de 100 mL de fenol (Riedel de Haen) con una concentración de 2000 ppm, luego se le añadió el catalizador LRS400 siendo lodo rojo (CVG-Bauxilim) neutralizado con salmuera de ósmosis inversa mejorada con cloruro de magnesio (Sigma-Aldrich y calcinado a 400 °C), a éste slurry se le ajustó el pH con ácido sulfúrico (Sigma-Aldrich) midiéndolo con un pHmetro digital Orión 330 Thermo, seguidamente al balón de reacción se le conectó un embudo de adición para la dosificación de peróxido de hidrógeno al 30 % (grado analítico marca Eka Nobel), además de un tubo de enfriamiento para el control de vapores generados y un termómetro (Fisherbrand) para el seguimiento de la temperatura de reacción, manteniendo una agitación constante a través de un agitador magnético (SLHS-SI Analytics) de acuerdo con el montaje experimental mostrado en la Figura 1.
Factores niveles y codificación del diseño de experimento factorial 23 con dos puntos al centro
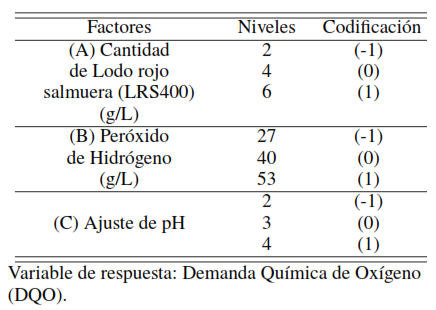

Figura 1
Montaje experimental del reactor para el proceso de oxidación avanzada
El tiempo de la reacción a la exposición solar se evaluó a 4h, en éste intervalo de tiempo se garantizó el cenit solar, la medición de la radiación solar (Wh/m2) se llevó a cabo mediante un piromanometro ISO First Class marca Climatronics Corporation, en las siguientes coordenadas Norte 10°22'03,16" y Este 67°02'38,25" a 1316 msnm, Los Teques, Estado Miranda-Venezuela.
Con las condiciones del mejor resultado obtenido en el diseño de experimento se desarrollaron los blancos del proceso de oxidación avanzada solar iniciando con la aplicación de un proceso Fenton-like, peroxidación con radiación solar (peroxidación/UV solar), fotolisis solar del fenol (fenol/ UV solar) y la aplicación del catalizador y radiación solar para medir su efecto en el fenol (fenol/CAT/UV solar).
Al finalizar la reacción se procedió a filtrar (filtro de papel Whatman) para separar las fases, envasando el líquido resultante en un vial ámbar en refrigeración con ausencia de luz, para finalmente determinar la DQO según el Método HACH DR2010, mientras la concentración de fenol se determinó por el método 4-aminoantipirina del Standard Methods 5530D (Modificada).
Se determinó el porcentaje de remoción o disminución de la DQO, mediante la ecuación (5):
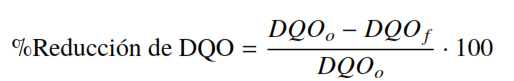 (5)
(5)Donde la DQOo es la DQO antes del proceso fotoquímico (mg O2/L) y la DQO f es el valor después del proceso. Los datos experimentales fueron analizados con el programa estadístico Statgraphic Centurion XVI, versión libre [24]. De la misma manera se determinó la disminución de la concentración de fenol en la reacción fotoquímica, así como para los blancos de la reacción mediante la ecuación (6):
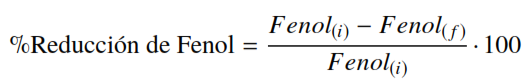 (6)
(6)Donde el Fenol(i) es la concentración inicial del proceso de reacción y el Fenol( f ) es el valor final de la fotoreacción. Para este análisis se realizó una curva de calibración del fenol mediante un espectrofotómetro HACH DR2010, aplicando la ley de Lambert-Beer.
La identificación de las especies de la degradación del fenol re realizó a través de la técnica de Cromatografía líquida de alta resolución (HPLC) acoplado a un detector UV-HP DAD, en un equipo marca Aligent Technologies serie 1200 con una columna C-18, 4,5mm, 3,5 µm, la fase móvil fue agua: metanol (Merk) en una proporción de 7:3 acidificada con ácido fosfórico (Scharlau AC 1100) hasta alcanzar un pH 4. Con el fin de garantizar la coincidencia espectral de los patrones secundarios utilizados en HPLC se empleó una cromatografía de gases acoplada a masas (CG-MS) bajo el método ASTM D5790-95 (2012) ensayo normalizado para medidas de compuestos orgánicos purgables en agua por columna capilar de cromatografía de gases/espectrometría de masa [25], se empleó un cromatógrafo de gases marca Agilent Technologies modelo 6890N acoplado a detector selectivo de masas Agilent Technologies 5973. Las especies de degradación del fenol que se utilizaron como patrón secundario fueron:
-
ácido acético glacial (JT Baker),
-
ácido fórmico (BDH Limited Poole England),
-
acido oxálico (Riedel de Haen),
-
hidroquinona (Fisher Scientific) y
-
fenol
3. Resultados y discusión
3.1. Caracterización de la muestra antes del tratamiento
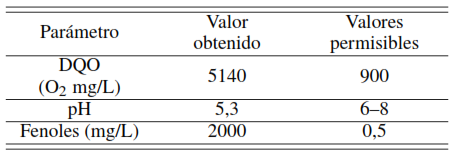
Según los resultados de los análisis químicos, los componentes de la muestra sintética inicialmente sobrepasan los límites de concentración permisibles para las descargas establecidas por la norma venezolana de aguas, según Decreto 883, 1995 [26], el cual establece las condiciones de descarga en efluentes y plantas de tratamientos para los contaminantes acuosos, tal como se observa en la Tabla 2. Donde se evidencia el carácter contaminante de este compuesto en solución y la necesidad de la aplicación de un tratamiento para poder ser descargado a los sistemas municipales e industriales de aguas servidas.
Caracterización de la muestra y los valores permisibles por la norma venezolana decreto 883
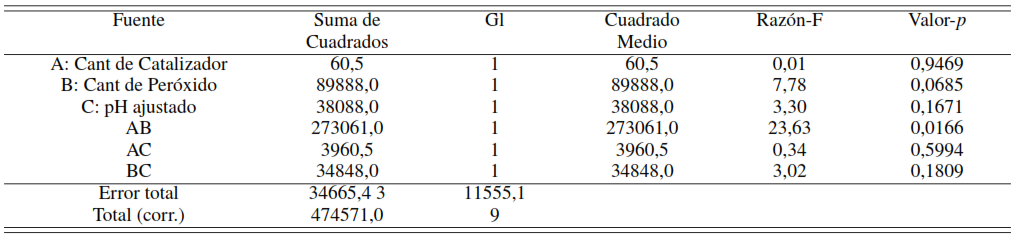
3.2. Análisis de Varianza para DQO diseño de experimento factorial 23con dos puntos al centro
En la Tabla 3 se muestra como solo la interacción lineal AB tiene un efecto significativo (p-valor: 0,0166) en la reducción de DQO, es decir, el catalizador lodo rojo neutralizado y calcinado (LRS400) en combinación con peróxido favorece la reducción de este parámetro por ende la de fenol, donde el catalizador es capaz de potenciar la generación de radicales libres en presencia del peróxido de hidrógeno [7]. La sinergia entre el catalizador (A) y el peróxido (B) es debido a la presencia de hierro (Fe+3), titanio (Ti) y manganeso (Mn) en el catalizador, los cuales tienen una actividad catalítica en conjunto con un agente oxidante como el peróxido de hidrógeno en los procesos de oxidación avanzada [27].
Por lo antes expuesto, el peróxido (valor-p: 0,0685) es de gran importancia por ser el agente oxidante en la reacción, a pesar de no haberse encontrado un efecto significativo en el ANOVA, de la misma forma no tienen relevancia la cantidad de catalizador (A valor-p 0,9469) y ajuste del pH (C valor-p 0,1671). Este DDE permitió obtener las condiciones de reacción para reducir la DQO de 5140 ppm a 300 ppm en un medio acuoso utilizando como catalizador lodo rojo activado para tratar una alta concentración de fenol.
Análisis de varianza para DQO para el diseño de experimento factorial 23 con dos puntos
En la Tabla 4 se muestran las corridas y las condiciones experimentales a las que fue sometida la solución de fenol, y se observa el tratamiento con mayor disminución de la DQO y del porcentaje de reducción de DQO. La variable de respuesta se redujo de la inicial 5140 mg O2/L a 300 mg O2/L, teniendo un porcentaje de reducción del 94,16 %, cuando se emplea la menor cantidad de peróxido, pero la mayor cantidad del catalizador (corrida 6), logrando de esta manera los valores más bajos en términos de la DQO. Estos resultados coinciden con los obtenidos por Atharizade y Miranzadeh [28] quienes lograron una disminución entre 82 y 97 % de la reducción de la DQO y la concentración de fenol utilizando una fuente de Fe+2 comercial, peróxido de hidrógeno y un ajuste de pH a 3. Por otra parte, Ramos y colaboradores [22] obtienen un 94 % a pH 2,5 y un 96 % a pH 1,6 con un catalizador MgFeAl y una concentración de Fenol con 11000 ppm.
DDE factorial 23 con dos puntos al centro y las variables de respuesta DQO y concentración de fenol, con sus respectivos blancos
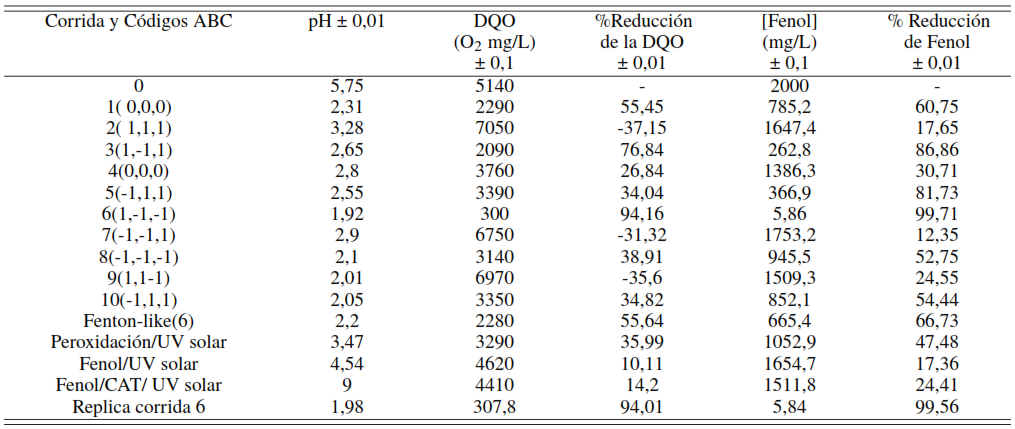
También se observa que al aumentar el pH a 3 (corrida 3) y trabajar con los niveles intermedios de las variables (corrida 1) se evidencia una reducción en la DQO reduciendo la concentración inicial de 2090 y 2290 mg O2/L respectivamente, esto valores representan un rendimiento aproximado de la reacción en un 76 y 55 %. Coincidiendo este último resultado con los obtenidos por Juzsakova y colaboradores [29] quienes trataron con ácido el lodo rojo para neutralizarlo seguido de una calcinación a 400 °C aumentando la conversión catalítica del etil-benceno hasta el 58 %.
El efecto que tiene el ajuste del pH en la reacción de POA es un indicador importante para determinar si la reacción de oxidación avanzada tiene un efecto positivo en la degradación o mineralización de un compuesto, debido a que una disminución considerable del pH, es indicativo de la formación de especies orgánicas oxidadas como los ácidos carboxílicos [30]. Los resultados muestran que una variación de pH por encima de 2, afecta el porcentaje de reducción, sin embargo, los resultados son buenos, un 55,45 % para un pH 3 y un 76,84 % para pH 4, estos resultados también dependen de la cantidad de catalizador y la cantidad de peróxido de hidrógeno. En esta investigación se tomó en cuenta que las reacciones de tipo fotoquímicas tienen un mejor desempeño a pH ácido [7, 31, 32].
A medida que se incrementa el pH existe un efecto que imposibilita la reacción de degradación. Para esto, se puede considerar el mecanismo propuesto para la fotodegradación de compuestos orgánicos con catalizadores que contienen Fe según Ramos [33] y Zhang y colaboradores [34]. Los autores antes mencionados consideran que el Fe+3 en la superficie del catalizador en presencia de la radiación se fotoreduce a Fe+2 (ecuación (4)), y con la adición del peróxido éste se aproxima al catalizador y reacciona en la superficie con el Fe+2 para producir radicales hidroxilos (ecuación (3)) [7, 8, 9]. Mientras más básico sea el pH del medio, la interacción entre el catalizador y la molécula del peróxido (con pares de electrones desapareados) es mínima debido a repulsión electrostática y por tanto no ocurrirá la interacción entre el peróxido de hidrógeno y el hierro en el catalizador, viendo este efecto en las corridas de los blancos fenol/UV solar con un pH cercano a 6, y la corrida con fenol/catalizador/UV solar con un pH de 9. A medida que se acidifica la solución, los sitios básicos son protonados (H+) formándose – M–OH2+ [33, 35], y de esta manera ocurre la aproximación entre el peróxido de hidrógeno y el catalizador para la producción del •OH, mejorando la degradación de la especie orgánica como en las corridas con pH 2 y 3. En este orden de ideas ha sido reportado que bajo pH ácido la superficie protonada de óxidos de hierro favorece la formación de complejos de esfera interna: óxido-fenol [33, 34].
Por lo tanto, las condiciones de pH en los procesos fotocatalíticos afectan notablemente este tratamiento ya que se han obtenido buenos resultados empleando TiO2 a diferentes rangos de pH, se han reportado excelentes rendimientos a pH ácidos [36]. Lo que hace suponer que éste compuesto en la superficie del catalizador realiza un aporte importante en la generación de radicales en el medio acuoso, fungiendo como un cocatalizador en el lodo rojo.
En esta investigación se consideraron como resultados positivos de la DQO a todos aquellos que logran una disminución del valor de DQO con respecto al valor inicial de la concentración de fenol (5140 ppm), tal y como ocurre en las corridas 1, 3, 4, 5, 6, 8, y 10 (Tabla 4). Por el contrario, el incremento de la DQO en las reacciones representan un valor negativo en el porcentaje del mismo, como se observa en las corridas 2, 7 y 9. El incremento de los valores de la DQO pueden deberse a que ocurran fotoreacciones incompletas realizando una polimerización del fenol, debido a que al iniciar la reacción entre el fenol y los radicales oxhidrilos se producen una serie de reacciones en la que dos o más radicales fenoxi se acoplan, dando lugar a la formación de otros intermediarios más complejos o polimerizados, tal y como lo afirman Mantilla y colaboradores [37], además de Ramos y colaboradores [38].
Cuando existe un exceso de peróxido en la reacción se experimenta una desmejora en la degradación de la materia orgánica debido a las reacciones inhibitorias y competitivas de los radicales generados por la descomposición del peróxido en exceso, como afirman Shu y colaboradores [39]; Primo [40], Centeno y Jiménez [7]. Esto explica los resultados obtenidos en las corridas 2, 5, 9 y 10 donde se incrementa considerablemente la cantidad de peróxido de hidrógeno, que lejos de lo que se puede pensar, no ocurre una significativa disminución de la DQO y de la concentración de fenol en las corridas 5 y 10, sino que más bien la muestra tiende a complejizarse y aumentar la cantidad de materia orgánica.
Por otra parte, bajo las condiciones experimentales de la corrida 6 se alcanza la menor concentración de fenol pasando de 2000 a 5,86 ppm de fenol, resultando en una fotodegradación de la molécula de un 99,71 %. Estos resultados evidencian que el lodo rojo neutralizado con salmuera y tratado térmicamente (LRS400) presenta especies en superficie que en presencia de un agente oxidante generarán especies radicales como el oxidrilo que permiten la degradación de los compuestos orgánicos específicamente del fenol a altas concentraciones. En la Tabla 4 también se evidencia el comportamiento en la reducción de fenol bajo las condiciones de las corridas 2, 7 y 9 pero la DQO no experimenta una disminución, lo cual pudiese deberse a la formación de especies transitorias complejas que no evidencian la reducción de la DQO [24, 37, 41].
Los blancos que se registran en la Tabla 4, permitieron analizar el comportamiento de cada subproceso de oxidación existente en la degradación de la especie molecular. El primer blanco se refiere al proceso Fenton-like(6), el cual consistió en aplicar las condiciones experimentales de la corrida 6, pero sin aplicar radiación solar. Evidenciándose en esta reacción POA no fotoquímico una reducción de la DQO equivalente al 55,64 % de la inicial y una reducción de la concentración de fenol en un 66,73 %, evidenciando la eficiencia de este tipo de POA. Estos resultados obtenidos con la reacción no fotoquímica Fenton-Like son inferiores a los obtenidos con la técnica fotoquímica, lo que evidencia que la fuente de radiación sobre la reacción incrementa sustancialmente la generación de radicales libres y en consecuencia mejora el rendimiento de la reacción fotoquímica considerablemente [9, 12, 42, 43].
La peroxidación (H2O2/UVsolar) es el segundo blanco donde se logró degradar la DQO en un 35,99 % y la concentración de fenol en un 47,4 % debido a la generación de radicales hidroxilo como consecuencia de la fotolisis del peróxido de hidrógeno [39, 40, 44]. Éste resultado corrobora la acción del oxidante en la generación de radicales libres permitiendo mejorar el rendimiento de la reacción y la eficiencia de la misma.
También se observa la fotolisis del fenol (fenol/UV) durante el periodo de tiempo de 4 h bajo condiciones de radiación solar, obteniéndose una fotolisis del fenol, con una disminución de la DQO 11,10 % y en cuanto al fenol en solución de 17,3 %. La exposición de la solución de fenol con el catalizador (fenol/cat), permitió obtener información del impacto que tiene el catalizador lodo rojo (LRS400) en condiciones de radiación solar para la disminución de las variables de respuesta. Bajo las condiciones experimentales de la corrida 6 en cuanto a la adición de la cantidad de catalizador, éste logró obtener resultados en la reducción de la DQO en un 14,20 % y en cuanto a la reducción en porcentaje de la concentración de fenol disminuyó en 24,41 %, esto pudiese deberse a la generación de radicales libres en medio acuoso del TiO2 [10, 11, 12, 13, 14, 15]. Así como también puede deberse a la acción del óxido férrico como un fotocatalizador tipo semiconductor [45, 46, 47, 48, 49].
3.3. Determinación de la coincidencia espectral de los patrones secundarios o los productos de degradación por Cromatografía de Gases Acoplada a Espectroscopia de Masa
Para la identificación por HPLC de los subproductos de la degradación de fenol, se generaron patrones secundarios a partir de reactivos comerciales disponibles en el laboratorio, y se les determinó su grado de coincidencia espectral mediante GC/MS. Los patrones fueron seleccionados de acuerdo a la reacción de oxidación de fenol con los procesos de oxidación avanzada, que conlleva a la hidroxilación de fenol a hidroquinona y catecol como un primer paso. Seguidamente ocurre una oxidación adicional de los hidroxilbencenos para formar benzoquinonas, que finalmente se degradan en ácidos orgánicos de cadenas cortas [41]. Por tanto, para la identificación de los subproductos se escogieron como patrones la hidroquinona y los ácidos acético, fórmico y oxálico. Adicionalmente se consideró el fenol, a fin de identificarlo en los casos donde no hubo una degradación completa.
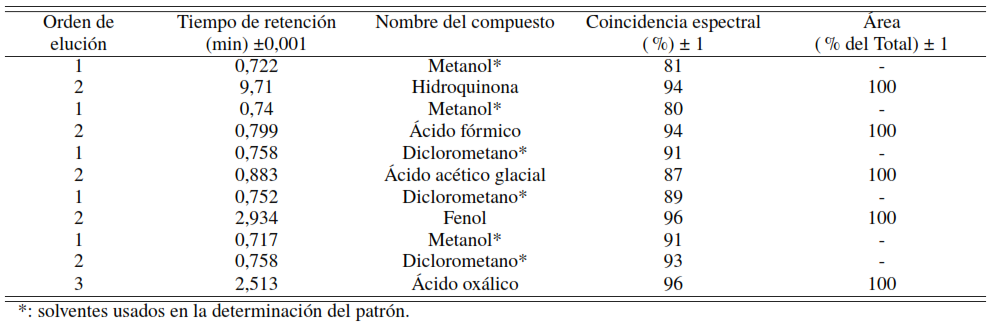
En la Tabla 5 se muestra el análisis realizado por GC/MS donde se identifican los compuestos mencionados encontrándose las siguientes coincidencias espectrales: fenol 96 %, ácido oxálico 95 %, hidroquinona 94 %, ácido fórmico 94 % y ácido acético 87 %. También se observan con un asterisco los solventes usados en la determinación del patrón, los tiempos de retención y el orden de elución de los compuestos. Estos resultaron permitieron obtener los patrones secundarios necesarios para identificar estas especies mediante HPLC en las muestras oxidadas por los POA aplicados a la solución de fenol.
Componentes de la muestra patrón por el método de compuestos orgánicos en mezclas complejas por GC-MS
3.4. Identificación de los productos de la degradación del fenol por Cromatografía Líquida de Alta Resolución (HPLC)
La identificación por HPLC de los subproductos de la degradación de fenol con lodo rojo se realizó mediante la preparación de soluciones madres de los ácidos oxálico, acético, fórmico, fenol e hidroquinona, con una concentración de 1000 ppm en metanol grado HPLC. En este sentido, se tomó la propuesta de Hasib y colaboradores [50]. Además de Ramos y colaboradores [30] donde utilizaron una fase móvil agua/metanol con un pH 4 obtenido con la adición de ácido fosfórico 0,1 M. Adicionalmente, se seleccionó una longitud de onda para la inyección de los patrones de 254 nm y 220 nm, obteniendo con ésta última los valores más altos de absorbancia para los patrones estudiados. Para determinar el flujo de la fase móvil se realizaron inyecciones de los patrones a 1, 0,5 y 0,25 mL/min y se compararon con los tiempos de retención.
La Figura 2 muestra la secuencia cromatográfica obtenida para la separación de los productos de degradación de fenol y de acuerdo a las condiciones operacionales optimizadas se analizaron las muestras patrones. El pico cromatográfico muestra primero al ácido oxálico eluyendo a un tiempo de retención de 3,061 min, seguido del ácido fórmico con un tiempo de 3,294 min, el ácido acético eluyó a 3,604 min, la hidroquinona fue el siguiente patrón en salir con un tiempo de 3,917 min y por último el fenol con un tiempo de retención de 11,270 min. Estos resultados presentan picos con tiempos de retención bien definidos entre sí.
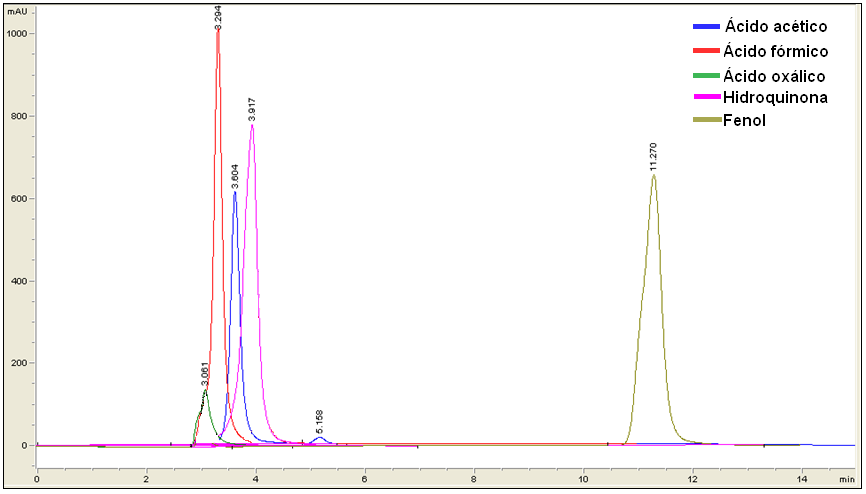
Figura 2
Cromatograma de los patrones estudiados
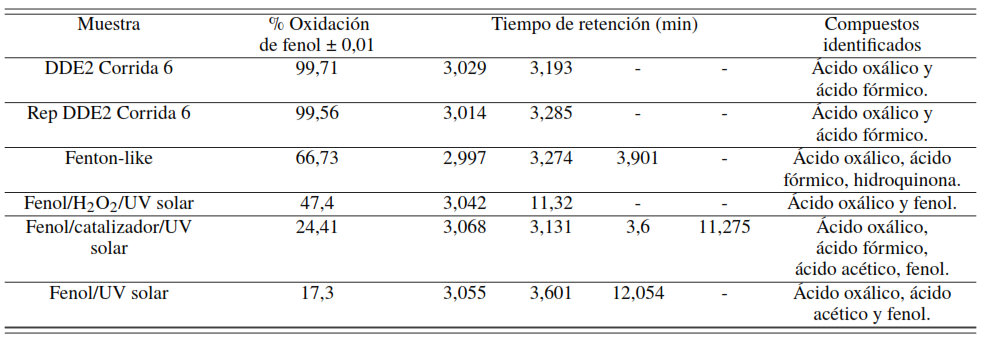
En la Tabla 6, se presentan las muestras tratadas y sus respectivos porcentajes de degradación en base a la concentración inicial y final del fenol y los tiempos de retención de los subproductos para el mejor resultado de las corridas experimentales y sus correspondientes blancos. De acuerdo a los resultados, en la degradación de las soluciones de fenol con POA solar, en la corrida 6 y su réplica se identificó por HPLC: ácido oxálico y fórmico, logrando una degradación a ácidos de cadena corta [50]. Adicionalmente, en el caso de la reacción Fenton-like donde se logró una degradación menor se identificó hidroquinona en las muestras. Se podría decir que la oxidación no fue tan directa, porque obtuvo mayor cantidad de subproductos de menor grado de oxidación, típica de los procesos de oxidación avanzada incompletas [24].
El análisis por HPLC mostró que la degradación de fenol con peróxido y UV solar, presentó ácido oxálico y fenol, mostrando que hubo oxidación, pero al mismo tiempo resulto no ser suficiente para la formación de radicales libres en la degradación completa del fenol. Por otra parte, La degradación de fenol con el catalizador lodo rojo LRS400 y radiación solar mostró que la degradación del fenol fue menor, observándose una oxidación incompleta en la identificación de ácidos oxálico, fórmico, acético y el remanente de fenol, propio de la oxidación incompleta de la reacción. Este resultado se debe a la generación de radicales libres fue únicamente por la acción de los óxidos tipo semiconductores presentes en el catalizador activados por la radiación solar [10, 11, 12, 13, 14, 15].
La fotolisis solar del fenol fue el proceso que obtuvo una menor oxidación porcentual del, con respecto a las especies identificadas por HPLC (ácido oxálico, ácido acético y fenol), lo que evidencia que la oxidación por esta vía es incompleta debido al fenol que no reaccionó.
Identificación de subproductos de la degradación de fenol con POA solar y lodo rojo como catalizador
3.5. Mecanismo de reacción propuesto para los POA solar con lodo rojo como catalizador
En la Figura 3 se observa el mecanismo de reacción propuesto para la degradación de fenol a partir de los POA solar y lodo rojo como catalizador. Este mecanismo surge de la revisión bibliográfica realizada con relación a la formación de especies de hidratación y de acuocomplejos del hierro en el lodo rojo, mediante lo propuesto por Jang y colaboradores [52] en combinación con los autores [7, 8, 9] para la graficar la interacción con la radiación solar y la formación de radicales oxhidrilo. En el mismo orden de ideas se representó la acción del óxido de titanio y su efecto en medio acuoso para la generación de radicales y la degradación de materia orgánica [10, 11, 12, 13, 14, 15]. La formación de radicales oxidrilo por vía fotoquímica y fotocatalítica sustenta el inicio al proceso de oxidación del fenol.
En el lodo rojo las principales especies fotoactivas que se encuentran son el óxido férrico (hematita) y el óxido de titanio (anatasa). La unidad estructural básica de la mayoría de los óxidos férricos (oxihidroxidos) es el octaedro donde Fe3+ se coordina a seis ligandos circundantes que pueden ser O2– , OH– y H2O [52]. En la primera fase, el complejo está compuesto por el sólido compuesto principalmente por O2– , siendo la estructura típica de la hematita (α–Fe2O3) [46]. Las condiciones de ajuste de pH de la reacción conducen a la segunda fase del complejo donde se evidencia la hidratación y la dilución del compuesto permitiendo la formación de un acuocomplejo [¨Fe3+L]n[52]. Esta especie compleja de Fe3+ sufre foto-reducción a una longitud de onda de 580 nm a través de una transferencia de carga-ligando-metal (LMCT) y los complejos intermediarios generados se disocian produciendo Fe2+, radical oxidrilo (•OH) y otros productos, tal como lo afirman [7, 24, 31, 53].
Por otra parte, el óxido de titanio (TiO2) se comporta como un semiconductor tipo óxido permitiendo la fotocatálisis heterogénea involucrando la absorción de la radiación en un amplio rango del espectro solar entre 200-620 nm, en específico el TiO2 tipo anatasa realiza una óxido-reducción generando un par electrón(e– )–hueco (h+).
Donde el electrón en la banda de valencia (bv) es excitado y promovido a la banda de conducción (bc). En la banda de valencia se genera un hueco (h+) que va reaccionar con el agua del medio permitiendo una foto-oxidación del agua produciendo el radical hidroxilo (•OH) y un protón al medio. En la banda de conducción el electrón excitado (e– ) va a producir la fotoreducción del peróxido de hidrógeno realizando una ruptura homolítica del mismo formando el radical hidroxilo (•OH) y este a su vez va reaccionar con el oxígeno del medio y va formar el radical superóxido (O2•) [10, 11, 12, 13, 14, 15].
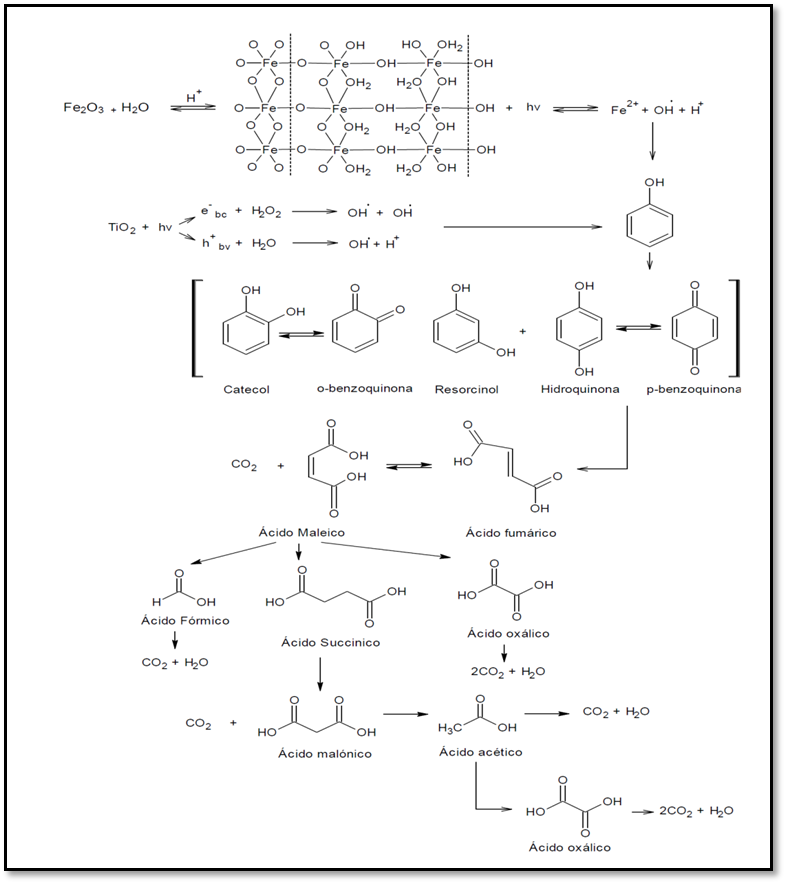
Figura 3
Mecanismo de reacción para la degradación de fenol mediante POA solar y lodo rojo como catalizador
La formación de radicales oxidrilo por vía fotoquímica y fotocatalítica son las especies que darán inicio al proceso de oxidación del fenol. Generalmente se considera que comienza la oxidación con una transferencia de electrones que conduce a la formación del radical fenoxi reaccionando este a su vez con el oxígeno del medio [54, 55]. Este radical fenoxi permite la hidroxilación formando los dihidoxilbencenos a través de los productos de sustitución del OH ortohidroxilación para la formación de catecol, metahidroxilación para el resorcinol y la parahidroxilación de la hidroquinona [56], que con una oxidación adicional y el correspondiente reeemplazo de los hidrógenos por grupos OH se forman las o-benzoquinonas y p-benzoquinonas tal y como afirman Eftaxias y colaboradores [51]. Por su parte, la apertura del anillo de la hidroquinona genera directamente ácidos insaturados como maleico y furmárico [56, 57]. Las benzoquinonas pueden ser degradadas a través del ácido 2,5-dioxo-3-hexenodioico, es decir sin pasar por el ácido maleico, debido a que este ácido es altamente reactivo y efímero, por lo que las benzoquinonas podrían producir directamente ácido oxálico [51].
El ácido oxálico se genera por el ataque del oxígeno al doble enlace carbono-carbono del ácido maleico para formar ácido oxálico, dióxido de carbono y agua [51]. El ácido fórmico se produce debido a una oxidación catalítica del ácido maleico [58]. El ácido maléico se reduce para formar el ácido succinico, y a su vez el ácido malónico, como ácido dicarboxílico sufre una descarboxilación para la formación de ácido acético, dióxido de carbono y agua [59, 60]. La formación del ácido oxálico a partir del ácido acético puede explicarse como una ruta de terminación en la oxidación por radicales libres del ácido acético. En este proceso, un radical hidroxilo ataca al compuesto alifático para eliminar un átomo de hidrógeno unido al carbono y los radicales libres [°COOH] para así formar el ácido oxálico [61]. Es importante resaltar que la formación de dióxido de carbono depende de la relación fenol /oxígeno produciéndose en cada paso desde el comienzo de la reacción, lo que indica que el mecanismo para la formación del dióxido de carbono debe ocurrir desde la reacción de hidroxilación [59].
4. Conclusiones
La degradación de fenol como molécula modelo utilizando oxidación avanzada solar y lodo rojo como catalizador fotoactivo, mostró excelentes resultados alcanzándose una disminución de la DQO del 94,1 % y 99,7 % de la concentración de fenol, lo cual pone en evidencia que los procesos de oxidación de tipo fotoquímico como el fotoFenton-like y la fotocatálisis a partir de un desecho metalúrgico activado es capaz de generar la suficiente producción de radicales hidroxilo en sinergia con el peróxido de hidrógeno para generar la degradación y mineralización del compuesto modelo. La técnica de GC/MS permitió seleccionar patrones secundarios con alta coincidencia espectral que garantizó la identificación de las especies orgánicas mediante la técnica HPLC. Las especies identificadas como principales productos de las reacciones fueron ácido oxálico y ácido fórmico en los casos de mayor degradación. Para los casos de menor porcentaje de degradación se determinó que el fenol quedaba remanente en la solución. Es relevante resaltar que la relación DQO: H2O2 es importante para lograr los mejores resultados de degradación y mineralización, utilizando esta técnica y el catalizador se logra disminuir la relación a la mitad de la reportada por la literatura.
5. Referencias
[1] G. Busca, S. Berardinelli, C. Resini, and L. Arrighi, “Technologies for the removal of phenol from fluid streams: a short review of recent developments,” Journal of Hazardous Materials, vol. 160, no. 2–3, pp. 265–288, 2008.
[2] M. Suárez-Ojeda, J. Carrera, I. Metcalfe, and J. Font, “Wet air oxidation (WAO) as a precursor to biological treatment of substituted phenols: Refractory nature of the WAO intermediates,” Chemical Engineering Journal, vol. 144, pp. 205–212,
[3] E. Garrido-Ramirez, B. Theng, and M. Mora, “Clays and oxide minerals as catalysts and nanocatalysts in Fenton-like reactions-A review,” Applied Clay Science, vol. 47, no. 3–4, pp. 182–192, 2010.
[4] J. Ñungo Moreno, J. Carriazo, S. Moreno, y R. Molina, “Degradación fotocatalítica de fenol empleando arcillas pilarizadas con Al – Fe y Al – Cu,” Revista de la Academia Colombiana de Ciencias Exactas, Físicas y Naturales, vol. 35, no. 136, pp. 295–302, 2011.
[5] G. López, R. García, y J. Orduña, “Estudio de la oxidación fotocatalítica de soluciones fenólicas, aplicando un proceso avanzado de oxidación (H2O2 / UV),” Ingenium, vol. 6, no. 12, pp. 61–67, 2012.
[6] M. Hincapié-Pérez, “La fotocatalisis en el tratamiento de aguas contaminadas,” Revista Ingenierías Universidad de Medellín, vol. 1, no. 1, pp. 83–91, 2002.
[7] G. Centeno y Y. Jiménez, “Uso de Lodos Rojos como catalizador en los procesos de oxidación avanzada: una aproximación al estado del arte,” Rev. Tekhné., vol. 21, no. 4, pp. 026–040, 2018.
[8] S. Malato, P. Fernández-Ibáñez, M. I. Maldonado, J. Blanco, and W. Gernjak, “Decontamination and disinfection of water by solar photocatalysis: recent overview and trends,” Catalysis today, vol. 147, no. 1, pp. 1–59, 2009.
[9] L. Doumic, “Nuevas estrategias para la oxidación catalítica de compuestos orgánicos en medio acuoso,” Tesis doctoral, Universidad de Buenos Aires, Buenos Aires, Argentina, 2015.
[10] O. Kartal, M. Erol, and H. Ouz, “Photocatalytic Destruction of Phenol by TiO2 Powders,” Chemical Engineering & Technology, vol. 24, no. 6, pp. 654–649, 2001.
[11] J. Pignatello, E. Oliveros, and A. MacKay, “Advanced oxidation processes for organic contaminant destruction based on the Fenton reaction and related chemistry,” Critical reviews in environmental science and technology, vol. 36, no. 1, pp.1–84, 2006.
[12] A. Babuponnusami and K. Muthukumar, “A review on Fenton and improvements to the Fenton process for wastewater treatment,” Journal of Environmental Chemical Engineering, vol. 2, no. 1, pp. 557–572, 2014.
[13] Q. Guo, C. Zhou, Z. Ma, Z. Ren, H. Fan, and X. Yang, “Elementary photocatalytic chemistry on TiO2,” Chemical Society Reviews, vol. 45, no. 13, pp. 3701–3730, 2016.
[14] D. Robert, N. Keller, and E. Selli, “Environmental photocatalysis and photochemistry for a sustainable world: a big challenge,” Environmental Science and Pollution Research International, vol. 24, pp. 12 503–12 505, 2017.
[15] M. Nevárez-Martínez, P. Espinoza-Montero, F. Quiroz-Chávez, y B. Ohtani, “Fotocatálisis: inicio, actualidad y perspectivas a través del TiO2,” Avances en Química, vol. 12, no. 45–59, pp. 2–3, 2017.
[16] R. C. Costa, F. C. Moura, P. E. Oliveira, F. Magalhães, J. D. Ardisson, and R. M. Lago, “Controlled. reduction of red mud waste to produce active systems for environmental applications: heterogeneous Fenton reaction and reduction of Cr (VI),” Chemosphere, vol. 78, no. 9, pp. 1116–1120, 2010.
[17] B. Galbičková, M. Soldán, M. Belčík, and K. Balog, “Removal Of Phenol From Wastewater By Using Low-Cost Catalyst From Metal Production,” Research Papers Faculty of Materials Science and Technology Slovak University of Technology, vol. 22, no. 341, pp. 55–59, 2014.
[18] M. Ma, G. Wang, Z. Yang, S. Huang, W. Guo, and Y. Shen, “Preparation characterization, and photocatalytic properties of modified red mud,” Advances in Materials Science and Engineering, vol. 2015, 2015.
[19] C. Gromboni, A. Ferreira, R. Nogueira, and A. Kamogawa, “Avaliacao da reacao fotofenton na descomposicao de residuos de carraticida,” Quimica nova, vol. 30, pp. 264–267, 2007.
[20] J. Sarasa, T. Llabrés, P. Ormad, R. Mosteo, and J. Ovelleiro, “Characterization and photo-Fenton treatment of used tires leachate,” Journal of Hazardous Materials, vol. 136, no. 3, pp. 874–881, 2008.
[21] D. Napoleão, R. Pinheiro, L. Zaidan, J. Rodríguez-Díaz, A. Araújo, M. Montenegro, and V. Silva, “Validation of a chromatographic method for amoxicillin determination in wastewaters after its degradation by advanced oxidation process,” Desalination and Water Treatment, vol. 57, no. 24, pp. 10 988–10 994, 2016.
[22] K. Ramos, Y. Jiménez, y C. Linares, “Síntesis y caracterización de óxidos: MgAl, MgFe, FeAl y MgFeAl para la degradación de fenol con foto-fenton solar.” Rev. LatinAm. Metal. Mat, vol. 35, pp. 315–325, 2016.
[23] E. Yamal-Turbay, E. Jaén, M. Graells, and M. Pérez-Moya, “Enhanced photo-Fenton process for tetracycline degradation using efficient hydrogen peroxide dosage,” Journal of Photochemistry and Photobiology A: Chemistry, vol. 267, pp.11–16, 2013.
[24] K. Ramos y Y. Jiménez, “Aplicación de diseño de experimentos en la degradación de desechos por el proceso foto-Fenton heterogéneo usando un óxido mixto de MgFeAl,” Saber, vol. 28, no. 3, pp. 574–582, 2016.
[25] American Society for Testing and Materials, ASTM D–5790–95. Standard Test Method for Measurement of Purgeable Organic Compounds in Water by Capillary Column Gas Chromatography/Mass Spectrometry, ASTM International, 2012.
[26] República Bolivariana de Venezuela, Gaceta Oficial Extraordinaria Nº 5.021. Decreto Nº 883, Normas para la Clasificación y Control de la Calidad de los Cuerpos de Agua y Vertidos o Efluentes Líquidos, Caracas, Venezuela, 1995.
[27] G. Centeno, Y. Jiménez, y J. V. García, “Caracterización fisicoquímica de los lodos rojos neutralizados y calcinados con posible actividad catalítica en procesos de oxidación avanzada,” Tekhné, vol. 23, no. 1, pp. 47–64, 2020.
[28] M. Atharizade and M. Miranzadeh, “Evaluation of efficacy of advanced oxidation processes Fenton, Fenton-like and photo-Fenton for removal of phenol from aqueous solutions,” J. Chem. Soc. Pak, vol. 37, no. 2, pp. 266–271, 2015.
[29] T. Juzsakova, A. Csavdari, Á. Rédey, T. Fráter, L. Dióssy, G. E. Popita, and J. Lauer, “Study on the alkylaton mechanism of isobutane with 1-butene using environmental friendly catalysts,” Environmental Engineering and Management Journal, 2014.
[30] K. Ramos, Y. Jiménez, M. C. Colmenares, L. Manganiello, y N. Mendoza, “Nota técnica: Identificación rápida de productos generados de la degradación por foto-Fenton solar mediante hplc con detección UV,” Revista Ingeniería UC, vol. 21, no. 1, pp. 87–92, 2014.
[31] A. Ribeiro, O. Nunes, M. Pereira, and A. Silva, “An overview on the advanced oxidation processes applied for the treatment of water pollutants defined in the recently launched Directive 2013/39/EU,” Environment International, vol. 75, pp. 33–51, 2015.
[32] M. Adán-Delgado, “Fotocatalizadores nanoestructurados de TiO2 y Fe – TiO2 para la degradación de compuestos aromáticos en medio acuoso empleando luz solar.” Tesis doctoral, Universidad Autónoma de Madrid. Facultad de Ciencias, 2015.
[33] K. Ramos, “Evaluación de procesos de oxidación avanzados: foto-fenton con luz solar para la degradación de sustancias y desechos líquidos tóxicos,” Tesis Doctoral, Universidad de Carabobo. Facultad de Ingeniería, 2018.
[34] S. Zhang, X. Zhao, H. Niu, Y. Shi, Y. Cai, and G. Jiang, “Superparamagnetic Fe3O4 nanoparticles as catalysts for the catalytic oxidation of phenolic and aniline compounds,” Journal of Hazardous Materials, vol. 167, pp. 560–566, 2009.
[35] S. Sable, F. Medina, and S. Contreras, “Clofibric acid degradation by catalytic ozonation using hydrotalcite-derived catalysts.” Applied Catalysis B: Environmental, vol. 150-151, pp. 30–36, 2014.
[36] S. H. S. Chan, T. Yeong Wu, J. C. Juan, and C. Y. Teh, “Recent developments of metal oxide semiconductors as photocatalysts in advanced oxidation processes (aops) for treatment of dye wastewater,” Journal of Chemical Technology & Biotechnology, vol. 86, no. 9, pp. 1130–1158, 2011.
[37] A. Mantilla, G. Jácome-Acatitla, G. Morales-Mendoza, F. Tzompantzi, and R. Gómez, “Photoassisted degradation of 4-chlorophenol and p-cresol using mgal hydrotalcites,” Industrial & Engineering Chemistry Research, vol. 50, no. 5, pp.2762–2767, 2010.
[38] K. Ramos, B. Sarrin, y Y. Jiménez, “Degradación de una mezcla de orto y para-nitrofenol mediante foto-fenton heterogéneo usando un óxido mixto de mgfeal como catalizador,” Revista Ingeniería UC, vol. 22, no. 2, pp. 37–45,2015.
[39] H. Y. Shu, H. J. Fan, M. C. Chang, and W. P. Hsieh, “Treatment of MSW landfill leachate by a thin gap annular UV/H2O2 photoreactor with multi-UV lamps,” Journal of Hazardous Materials, vol. 129, no. 1–3, pp. 73–79, 2006.
[40] O. Primo, “Mejoras en el tratamiento de lixiviados de vertedero de RSU mediante procesos de oxidación avanzada,” Tesis doctoral, Universidad de Cantabria, 2009.
[41] F. Stüber, J. Font, A. Fortuny, C. Bengoa, A. Eftaxias, and A. Fabregat, “Carbon materials and catalytic wet air oxidation of organic pollutants in wastewater,” Topics in Catalysis, vol. 33, no. 1–4, pp. 3–50, 2005.
[42] N. Mahamuni and Y. Adewuyi, “Advanced oxidation processes (AOPs) involving ultrasound and UV for waste water treatment: A review with emphasis on cost estimation,” Ultrasonics Sonochemistry, vol. 17, pp. 990–1003, 2010.
[43] A. Soon and B. Hameed, “Heterogeneous catalytic treatment of synthetic dyes in aqueous media using Fenton and photo-assisted Fenton process,” Desalination, vol. 269, no. 1–3, pp. 1–16, 2011.
[44] P. Gogate and A. Pandit, “A review of imperative technologies for a waste wáter treatment I: oxidation technologies et ambient conditions,” Advanced in Enviromental Research, vol. 8, no. 3–4, pp. 501–551, 2004.
[45] M. Hoffman, S. Martin, W. Choi, and W. Bahnemann, “Enviromental applications of semiconductor photocatalysis,” Chem. Rev, vol. 95, no. 1, pp. 69–96, 1995.
[46] Q. Wu, X. Hu, and P. Yue, “Mechanistic and kinetic studies of heteroheneus UV/fenton process for the oxidation of aquous organic pollutants: electron transfer at catalyst surface to initiate the redox process,” Hong kong productivity council, vol. 15, no. 5, pp. 112–122, 2006.
[47] R. Shawabkeh, O. Khashman, and G. Bisharat, “Photocatalytic degradation of phenol using Fe – TiO2 by different illumination sources,” International Journal of Chemistry, vol. 2, no. 2, pp. 10–18, 2010.
[48] F. Martín, M. Cruz-Yusta, L. Sánchez, y J. Balbuena, “Nanofibras de hematita (α – Fe2O3) para la eliminación de gases NOx mediante fotocatalisis,” en V Encuentro de Nanociencia y Nanotecnología de Investigadores y Tecnólogos Andaluces, Córdoba, España, 2015.
[49] A. Rubio, E. Chica, y G. Peñuela, “Aplicación del proceso Fenton en el tratamiento de aguas residuales de origen petroquímico,” Ingeniería y competitividad, vol. 16, no. 2, pp. 211–223, 2014.
[50] A. Hasib, A. Jaouad, M. Mahrouz, and M. Khouili, “HPLC determination of organic acids in moroccan apricot,” CYTA-Journal of Food, 2002.
[51] A. Eftaxias, J. Font, A. Fortuny, J. Giralt, A. Fabregat, and F. Stüber, “Kinetic modelling of catalytic wet air oxidation of phenol by simulated annealing,” Applied Catalysis B: Environmental, vol. 33, no. 2, pp. 175–190, 2001.
[52] J. Jang, B. Dempsy, and W. Burgos, “Solubility of hematite revisited: effects of hidratation,” Environmental Science & Technology, vol. 41, no. 21, pp. 7303–7308, 2007.
[53] J. Amigó, “Caracterización de la degradación de sulfametazina mediante foto-fenton (POA’s),” Tesis doctotal, Universidad Politecnica de Catalunya, España, 2008.
[54] H. Lund and M. Baizer, Organic Electrochemistry: An Introduction and a Guide, 3rd ed. New York: Marcel Dekker Inc, 1991.
[55] X. Y. Li, Y. H. Cui, Y. J. Feng, Z. M. Xie, and J. D. Gu, “Reaction pathways and mechanisms of the electrochemical degradation of phenol on different electrodes,” Water research, vol. 39, no. 10, pp. 1972–1981, 2005.
[56] T. Olmez-Hanci and I. Arslan-Alaton, “Comparison of sulfate and hydroxyl radical based advanced oxidation of phenol,” Chemical Engineering Journal, vol. 224, pp. 10–16, 2013.
[57] J. Zazo, J. Casas, A. Mohedano, M. Gilarranz, and J. Rodríguez, “Chemical pathway and kinetics of phenol oxidation by Fenton’s reagent,” Environmental science & technology, vol. 39, no. 23, pp. 9295–9302, 2005.
[58] A. Santos, P. Yustos, A. Quintanilla, S. Rodríguez, and F. García-Ochoa, “Route of the catalytic oxidation of phenol in aqueous phase,” Applied Catalysis B: Environmental, vol. 39, no. 2, pp. 97–113,
[59] H. R. Devlin and I. J. Harris, “Mechanism of the oxidation of aqueous phenol with dissolved oxygen,” Industrial & engineering chemistry fundamentals, 1984.
[60] X. Li, Y. Cui, Y. Feng, Z. Xie, and J. Gu, “Reaction pathways and mechanisms of the electrochemical degradation of phenol on different electrodes,” Water research, vol. 39, no. 10, pp. 1972–1981, 2005.
[61] L. Pernía, “Aplicabilidad del percarbonato de sodio obtenido de un pasivo ambiental en la oxidación de fenol en fase acuosa,” Trabajo especial de grado, Magister Scientiarum en Ingeniería Sanitaria Mención Calidad de Agua, Universidad Central de Venezuela, 2019.
Notas de autor
gcenteno1@uc.edu.ve
Enlace alternativo
http://servicio.bc.uc.edu.ve/ingenieria/revista/v27n2/art03.pdf (pdf)
