Artículos

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial 4.0 Internacional.
Recepción: 22 Agosto 2020
Aprobación: 20 Enero 2021
Publicación: 01 Diciembre 2021
Resumen: Los baculovirus son patógenos aislados de insectos, principalmente del orden Lepidoptera. Se caracterizan por su alta especificidad, pues poseen un espectro de hospedadores reducido, y por ser inocuos para artrópodos benéficos, plantas y mamíferos. Estas características les confieren a los baculovirus propiedades óptimas para su uso como bioinsecticidas. Su aplicación permite el control de plagas claves en cultivos de lechuga, tomate, berenjena, morrón y maíz en elevados porcentajes de efectividad. El empleo de estos agentes en la horticultura va en aumento a nivel regional. En Latinoamérica su utilización se asocia principalmente a sistemas hortícolas con producción orgánica. En la Argentina se han caracterizado numerosos aislamientos baculovirales autóctonos que poseen un alto potencial para su aplicación como bioinsecticidas en el control de plagas presentes en sistemas hortícolas. La incorporación de estos agentes en programas de manejo de plagas permite disminuir el uso de insecticidas sintéticos y minimizar el impacto negativo sobre alimentos de consumo humano y el ambiente.
Palabras clave: control biológico, control de plagas, bioinsecticidas, horticultura.
Abstract: Baculoviruses are pathogenic viruses isolated from insects mainly included in the order Lepidoptera. These viruses have a high host-specificity, with no effects on non-target insects, plants or vertebrates. Baculoviruses are an effective tool for insect pest management. These bioinsecticides allow farmers to control key pests in lettuce, tomato, eggplant, bell pepper and corn crops with high percentages of effectiveness. The use of baculovirus-based pesticides in horticulture is increasing at regional level. In Latin America these types of bioinsecticides are used in horticultural systems with organic production. In Argentina, new indigenous baculovirus isolates were characterized and most of them demonstrated a high potential for application as bioinsecticides to control horticultural pests. The incorporation of baculovirus in pest management programs decrease the use of synthetic insecticides and their negative impact on food for human consumption and the environment.
Keywords: biological control, pest control, bioinsecticides, horticulture..
INTRODUCCIÓN
Entre las diferentes herramientas utilizadas en el control de plagas agronómicas, el uso de microorganismos representa una alternativa eficaz y de bajo impacto ambiental (Deshayes et al., 2017). Los virus de insectos denominados baculovirus (Fam. Baculoviridae) poseen el mayor número de agentes con potencial para ser utilizados en el desarrollo de insecticidas biológicos (Lacey et al., 2015). En la actualidad se cuenta en el mundo con más de 80 productos comerciales elaborados sobre la base de unos quince baculovirus diferentes (Afolami y Oladunmoye, 2017; Grzywacz y Moore, 2017). Los baculovirus fueron aislados exclusivamente de artrópodos, los cuales en su mayoría están incluidos en la clase Insecta y el orden Lepidoptera (Theilmann et al., 2005). Los aislamientos baculovirales presentan un reducido espectro de hospedantes y su aplicación como bioinsecticidas no produce daño sobre plantas, insectos benéficos y mamíferos incluyendo al hombre (Gröner, 1986). Durante su ciclo de replicación, este grupo de virus forman unas estructuras proteicas (cuerpos de oclusión) en las cuales se alojan los viriones infectivos (Rohrmann, 2019). Estas partículas microscópicas, del orden del micrómetro de tamaño, pueden ser fácilmente aplicables mediante pulverizadores tradicionales, permanecer estables en el ambiente varios meses (principalmente en suelo y hojas) y, por lo tanto, servir como inóculo infectivo a poblaciones de insectos susceptibles (Granados y Federici, 1986).
Entre los baculovirus que se han empleado comercialmente a nivel regional para el control de plagas agrícolas se destacan entre otros, el virus aislado de la oruga de las leguminosas (Anticarsia gemmatalis) denominado AgMNPV. Este virus fue incorporado en los programas de protección vegetal del cultivo de soja en Brasil y aplicado en casi dos millones de hectáreas (Moscardi y Sosa-Gómez, 1992). Otro ejemplo destacado es el del baculovirus aislado de carpocapsa o polilla del manzano (Cydia pomonella) llamado CpGV (Jaques et al., 1987). Este bioinsecticida se utiliza para el control de este lepidóptero en cultivos de manzana, pera, membrillo y nuez. Se estima que a nivel mundial unas 100.000 ha son tratadas anualmente con este virus (Lacey et al., 2008a). En la Argentina, el Instituto Nacional de Tecnología Agropecuaria (INTA) registró el primer formulado de CpGV en el año 2000, y su uso se ha extendido de manera lenta pero sostenida en el sector frutícola. Así, cada año se tratan con este virus entre 3000 a 5000 ha de frutales en las regiones productoras de Patagonia y Cuyo (Quintana y Alvarado, 2004).
A diferencia de la agricultura extensiva, la horticultura se distingue por mostrar diferentes prácticas especializadas según el cultivo, pero principalmente por la pequeña escala de las tareas y la superficie en que se desarrolla (Leguizamón, 2018). En la actualidad, debido al impulso de la producción orgánica de alimentos humanos y la tendencia a la disminución del empleo de plaguicidas de síntesis, el uso de los baculovirus ha tomado impulso como alternativa sustentable. En este trabajo se presentan características moleculares, biológicas y ejemplos de baculovirus usados para el control exitoso de plagas claves en cultivos hortícolas en Latinoamérica.
Estructura y biología de los baculovirus
A nivel estructural, los baculovirus poseen un genoma de ADN doble cadena, circular, que varía entre 80 y 180 kpb y codifica entre 90 y 180 genes (Kelly et al., 2016). Durante su ciclo infectivo se diferencian dos tipos de viriones genéticamente iguales, pero morfológicamente diferentes: los viriones ocluidos (occluded virions, OVs), los cuales se encuentran incorporados en una matriz proteica que constituye los denominados cuerpos de oclusión (occlusion bodies, OBs) (figura 1). El segundo tipo de virión son los denominados viriones brotantes (budded virions, BVs), los cuales se generan luego del primer ciclo de replicación del virus dentro del hospedador y son los encargados de dispersar la infección a diferentes células y tejidos (Theilmann et al., 2005). De esta forma, los dos tipos de viriones cumplen funciones diferentes durante el ciclo biológico del patógeno.

Figura 1
Cuerpos de oclusión baculovirales (OBs). Izquierda: poliedros de Autographa californica Multiplenucleopoliedrovirus (AcMNPV). Derecha: gránulos de Epinotia aporema Granulovirus (EpapGV).
(Fotos obtenidas por microscopía electrónica de barrido. Ricardo Salvador).El ciclo infectivo de los baculovirus se divide en dos etapas: la infección primaria y la infección secundaria (figura 2). En la primera etapa, las larvas ingieren los cuerpos de oclusión (OBs) que se encuentran en el ambiente contaminando su alimento, principalmente hojas, tallos o frutos. Estos OBs ingeridos, al alcanzar el intestino medio de la larva, son disueltos permitiendo la liberación de los viriones derivados de los cuerpos de oclusión (ODV). Los viriones atraviesan la membrana peritrófica, que reviste internamente el intestino, la cual alteran mediante proteínas asociadas a los cuerpos de oclusión (Rohrmann, 2019). Luego, se unen a las microvellosidades del epitelio intestinal mediante la fusión de sus membranas y las nucleocápsides (NC) contenidas en el interior del virión, las cuales son liberadas en el citosol (Blissard y Theilmann, 2018). Estas NC son transportadas al núcleo iniciando la replicación del ADN y la transcripción de las proteínas virales que permite la formación de nuevas NCs.
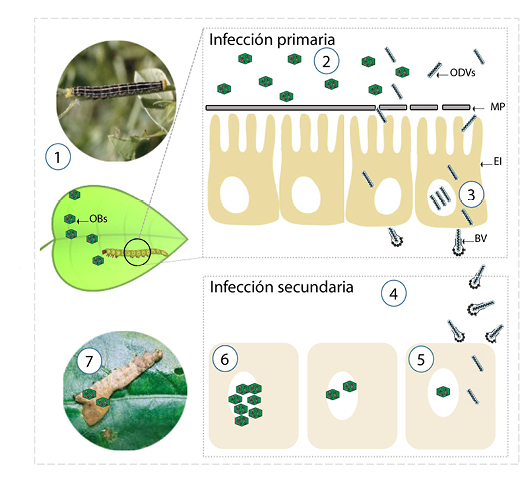
Figura 2
Ciclo de infección de baculovirus.1. Los cuerpos de oclusión de los baculovirus (OBs) son ingeridos por el estadio larval debido a que se encuentran contaminando su alimento (hojas, tallos y frutos). 2. En el intestino medio, los OBs se disuelven debido a la acción de proteasas intestinales y liberan los viriones (ODVs). La membrana peritrófica (MP) que recubre el epitelio intestinal (EI) es degradada por enzimas asociadas a los OBs permitiendo la entrada de los ODVs a las células intestinales. 3. En el epitelio intestinal los ODV pueden iniciar un ciclo de replicación generando el fenotipo de los viriones brotantes (BV) o alternativamente dirigirse hacia la membrana basal del epitelio y salir de la célula como BV. 4. Se inicia la infección secundaria hacia otros tejidos del hospedador. 5. Los BV replican su material genético y comienza la síntesis de la proteína que constituye los cuerpos de oclusión, formándose de esta forma los OBs. 6. En etapas finales del ciclo, las células se encuentran con una gran cantidad de OBs. 7. Al morir la larva como consecuencia de la infección viral, los OB son liberados al medio contaminando las fuentes de alimentación del estadio larval de los hospedadores.
En la etapa secundaria de la infección, las NCs formadas son transportadas hacia la membrana celular, desde donde emergen de la célula por brotación o a través de la membrana basal. Así, se conforman los viriones brotantes (BV) que migran a células vecinas y son los responsables de infectar otros tipos celulares o tejidos susceptibles. Avanzada esta etapa, se empiezan a constituir los cuerpos de oclusión (OBs), debido a que la proteína que lo compone (poliedrina o granulina) se sintetiza en grandes cantidades y se acumula rodeando a los viriones (Theilmann et al., 2005). Al finalizar esta etapa se produce la lisis celular, adquiriendo el insecto una coloración blanquecina debido a la acumulación de los OBs. Luego, el tegumento de la larva muerta se rompe y se liberan los OBs en el ambiente, reiniciando el ciclo cuando larvas de insectos susceptibles ingieren alimento contaminado con estos (Rohrmann, 2019).
El suelo es considerado el principal reservorio de baculovirus en el ambiente (Kelly et al., 2016). Los cuerpos de oclusión (OBs) pueden permanecer viables durante largos periodos (meses o años), dependiendo de las condiciones ambientales y las características fisicoquímicas del suelo. En general, los OBs persisten mejor en suelos ácidos o neutrales, mientras que condiciones como la exposición a radiación ultravioleta o ambientes alcalinos suelen reducir considerablemente la viabilidad del virus (Fuller y Dwyer, 2012). También, se ha comprobado que ciertos genotipos virales están mejor adaptados a la persistencia en el ambiente que otros (Murillo et al., 2007). Todos estos factores son considerados con el fin de optimizar la utilización de los baculovirus en el control de plagas.
Uso de los baculovirus como bioinsecticidas
Dentro del control biológico, el uso de agentes entomopatógenos se realiza mediante la estrategia aumentativa, la cual consiste en incrementar la presencia del agente de biocontrol en el ambiente (Lacey, 2016). A su vez, dentro de esta estrategia, para el uso de virus, bacterias y hongos se emplea la variante inundativa, la cual requiere de la introducción periódica del patógeno en el medio donde se encuentra la plaga. De esta forma se intenta asegurar en el medio una concentración adecuada del virus que sea capaz de controlar de forma significativa a la población blanco. En esto último es determinante la patogenicidad del aislamiento, la cual es esencial para reducir el tiempo en el cual el insecto muere desde la ingestión del virus. Cuanto más virulento es el aislamiento, menor será el daño de la plaga sobre el cultivo (Lacey et al., 2001).
Una vez establecida la eficacia de un aislamiento como agente de control es posible multiplicarlo y combinarlo con un soporte sólido o líquido que optimice su aplicación y conservación, proceso conocido como formulación (Grzywacz y Moore, 2017). A partir de los formulados comerciales, en polvo mojable o en suspensión líquida, los productos solo requieren para su aplicación ser disueltos en agua a un pH neutro. También, según las condiciones ambientales en las cuales se aplique el producto (humedad, precipitaciones, vientos, etc.), la mezcla acuosa puede requerir de la adición de algún compuesto adherente o protector contra la radiación ultravioleta (Haase et al., 2015).
Durante el periodo comprendido entre la producción del formulado y el momento de aplicación, el producto no debe experimentar una pérdida significativa en su viabilidad. Esta última puede verse afectada por la descomposición de los componentes de la formulación, por cambios en la composición física del formulado (por sedimentación o agregación de virus en suspensiones), y en el caso de formulaciones a base de polvos mojables, por el resecamiento y endurecimiento de estos (Couch e Ignoffo,1981). Para asegurar la actividad biológica de los agentes virales deben evitarse las temperaturas elevadas ya que alteran por desnaturalización los componentes proteicos del virus. Por lo tanto, es fundamental mantener la cadena de frío durante la etapa de distribución para asegurar la viabilidad del producto (Jarvis y Garcia, 1994).
Los formulados actualmente disponibles se caracterizan por su gran estabilidad ante periodos prolongados de almacenamiento (Tamez-Guerra et al., 2002; Behle et al., 2003). Por ejemplo, a una temperatura de 4 °C pueden mantenerse activos hasta dos años, mientras que el almacenamiento por debajo de esa temperatura puede extender aún más el tiempo de viabilidad del producto (Jarvis y Garcia, 1994). Por ejemplo, el producto comercial Tutavir®, utilizado para el control de la polilla del tomate Tuta absoluta, puede mantenerse viable durante dos años a una temperatura de almacenamiento de 5 °C (Boletín de información técnica Tutavir®, 2020). Otro estudio demostró que una formulación del virus CpGV conservada a -18 °C durante 3 años, mantiene la misma efectividad insecticida que una preparación reciente de virus (Lacey et al., 2008b).
Debido a la naturaleza particulada de los cuerpos de oclusión infectivos, las formulaciones pueden ser aplicadas sobre los cultivos empleando los pulverizadores tradicionales utilizados con insecticidas químicos (Boletín de información técnica Gemstar®, 2020). También, el formulado puede ser aplicado mediante sistemas de riego automático por aspersión, el cual favorece una correcta cobertura del follaje de las plantas (Valicente y Costa, 1995). La frecuencia de las aplicaciones dependerá de la virulencia del agente utilizado, la presión de la plaga sobre en el cultivo y las condiciones del medioambiente. Así, las pulverizaciones pueden realizarse en intervalos que van de los 3-5 días hasta los 14 días o más, dependiendo del nivel de incidencia de la plaga.
Otra característica ventajosa de los baculovirus, en relación con su aplicación, es su compatibilidad con otros plaguicidas como insecticidas, fungicidas y reguladores de crecimiento o abonos foliares, siempre que el pH de estos se mantenga en valores cercanos a la neutralidad (Boletines de información técnica Littovir®, Tutavir®, Loopex®, Helicovex® y VPN Ultra®, 2020). Esto permite el empleo de los baculovirus en forma simultánea con otro tipo de productos utilización de común en sistemas hortícolas.
En relación con la eficacia de control de los productos comerciales a base de baculovirus, se puede mencionar que esta depende de la concentración del virus empleada, el cultivo, las condiciones ambientales y la plaga. Por ejemplo, bioinsecticidas baculovirales utilizados para el control del lepidóptero Spodoptera exigua tienen una eficacia de control con valores cercanos a un 80% cuando es aplicado sobre el cultivo de lechuga, y de un 100% cuando es empleado para controlar a esta plaga en el cultivo morrón (Lasa et al., 2007; Boletín de información técnico Spexit®, 2020) (figura 3). Los productos comerciales disponibles en la actualidad permiten porcentajes de control de las plagas blancos que oscilan entre un 70% y 100%, dependiendo de las condiciones citadas anteriormente.
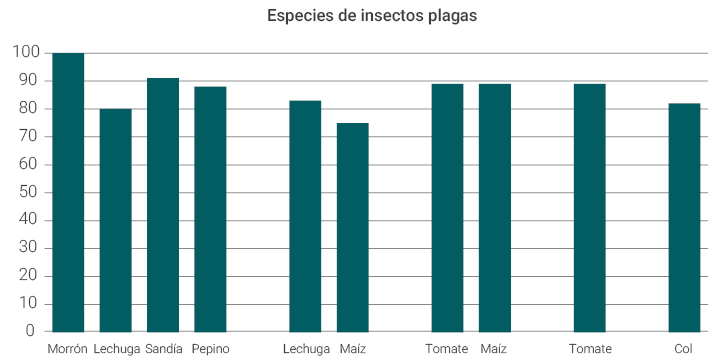
Figura 3
Eficacia de baculovirus. Principales insectos plagas encontrados en cultivos hortícolas y porcentajes de control alcanzados mediante el uso de formulaciones comerciales a base de baculovirus.
(Fuente: Lasa et al.,2007; Valicente y Costa, 1995, Arrizubieta et al., 2015; boletines de información técnica de productos Littovir®, Tutavir®, Loopex® y Helicovex®).La utilización de estos productos, ya sea a campo o en invernáculo, se asocia generalmente a una producción de tipo orgánica que, si bien eleva los costos de mantenimiento del cultivo, también aumenta el valor de comercialización cuando se compara con la producción hortícola tradicional que emplea insecticidas químicos.
Uso regional de baculovirus en horticultura
La horticultura se diferencia de otro tipo de agricultura por emplear una amplia diversidad de técnicas especializadas según el cultivo y, principalmente, por la pequeña escala de las tareas y la superficie en que se desarrolla (Leguizamón, 2018). Esto último representa una ventaja para la utilización de agentes baculovirales en el control de plagas presentes en cultivos hortícolas. Si bien la utilización de estos agentes de biocontrol es incipiente a nivel regional, existen numerosos ejemplos de su aplicación exitosa para el control de plagas claves en horticultura.
Desde México hasta en países sudamericanos como Colombia, Ecuador, Perú, Bolivia y Brasil se emplean baculovirus capaces de generar un control efectivo sobre plagas claves encontradas en cultivos como morrón, tomate, lechuga, maíz dulce, mandioca, berenjenas y papa (Haase et al., 2015) (figura 4).
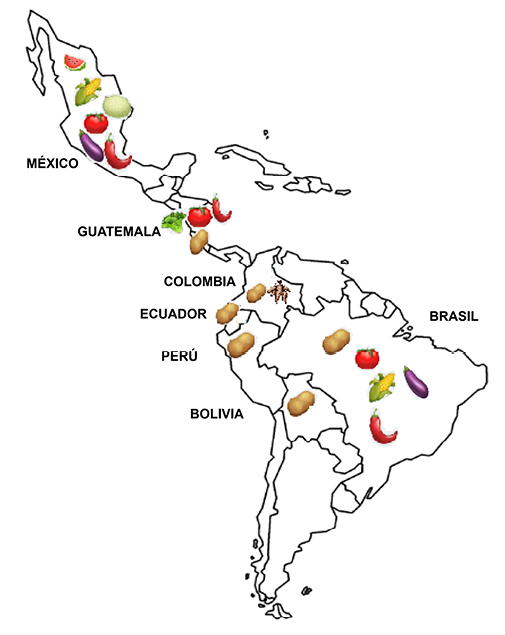
Figura 4
Uso regional de baculovirus. Países latinoamericanos y cultivos hortícolas en los cuales son empleados bioinsecticidas a base de baculovirus para el control de plagas claves.
En Latinoamérica, un total de 8 baculovirus diferentes son empleados en formulaciones comerciales para controlar 20 plagas claves en cultivos hortícolas (tabla 1). Estos bioinsecticidas pueden ser utilizados en combinación con insecticidas químicos (Dader et al., 2020), otro tipo de agentes de control microbianos como la bacteria Bacillus thuringiensis (Bt) (Han et al., 2015), u hongos entomopatógenos como Beauveria bassiana o Metarhizium anisopliae (Pauli et al., 2018). Estos últimos, ampliamente utilizados para el control de hormigas y chinches, entre otros artrópodos perjudiciales (Mascarin et al., 2019).
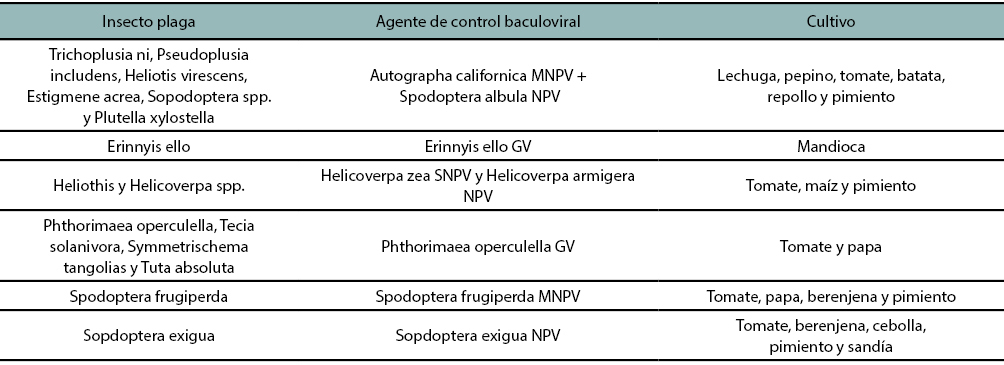
Tabla 1
Baculovirus incluidos en formulaciones comerciales en Latinoamérica para el control de plagas presentes en cultivos hortícolas.
(Fuente: Hasse et al.,2015. Boletines técnicos de Littovir®, Tutavir®, Loopex®, Helicovex® y VPN-ULTRA®).A nivel mundial existe un incremento sostenido en la producción y uso de bioinsecticidas (Glare et al., 2016). En esta década, la utilización de esta clase de bioinsumos registró un incremento anual del 15% a nivel global (Pelaez y Mizukawa, 2017). Los virus entomopatógenos, hasta el momento solo representan el 5% del mercado de comercialización mundial (Mishra et al., 2015). En Latinoamérica, el mercado se concentra principalmente en el uso de los bioplaguicidas microbianos a base de B. thurigensis (Bt) y de hongos (micoplaguicidas), con un valor de 41% y 49%, respectivamente (Bautista et al., 2018). El porcentaje de comercialización de los baculovirus es similar al estimado a nivel global (Mishra et al., 2015), aunque no existen datos precisos que indiquen el uso de estos en sistemas hortícolas.
Aislamientos locales de baculovirus con elevada patogenicidad en plagas presentes en horticultura
En Argentina, se realizaron diferentes aislamientos baculovirales con elevada capacidad insecticida sobre sus hospedadores y, por lo tanto, con potencial para ser utilizados como bioinsecticidas. Entre estos, se pueden mencionar los aislamientos obtenidos del lepidóptero S. frugiperda denominados como SfMNPV y SfGV, los cuales fueron caracterizados a nivel biológico y molecular (Berretta et al., 1998; Ferrelli et al., 2018; Pidre et al., 2019; Niz et al., 2020). Estudios preliminares muestran que la combinación en mezclas del virus SfMNPV con el virus de la granulosis SfGV produce una elevada y rápida mortalidad en larvas de S. frugiperda (Cuartas-Otalora et al., 2019). Así, esta mezcla con ambos agentes virales evidencia ser un potente bioinsecticida, el cual podría ser utilizado en el control de esta plaga polífaga con una elevada presencia en los principales cultivos hortícolas.
Recientemente, se aisló de la oruga Helicoverpa gelotopoeon, un baculovirus altamente patogénico, el cual fue denominado HearSnPV (Ferrelli et al., 2016). Los ensayos realizados en H. gelotopoeon demostraron que la administración oral de poliedros de HearSNP es capaz de producir una mortalidad del 91% en larvas infectadas. Los resultados obtenidos hasta el momento indican que el aislamiento es un buen candidato viral para ser utilizado como bioinsecticida en el control de orugas bolilleras presentes en cultivos hortícolas como maíz dulce, tomates, morrón y lechuga entre otros.
Dos aislamientos nativos a partir del lepidóptero Rachiplusia nu se están caracterizando y evaluando bajo condiciones de laboratorio. Uno de ellos es un baculovirus clasificado como RanuMNPV, que podría considerarse una variante de Autographa californica MNPV, el cual presenta un amplio rango de hospedadores diferente (Rodríguez et al., 2012.). El otro aislamiento denominado RanuSNPV parece ser un virus aún no descrito en la literatura, pero con alto potencial como bioinsecticida (Jakubowicz et al., 2019). Estos aislamientos podrían emplearse en el control de este lepidóptero, el cual causa importantes daños mediante defoliación en cultivos como arveja, papa, tomate, poroto, zapallo y espinaca, en los cuales produce importantes daños mediante defoliación.
CONCLUSIONES
Los baculovirus demuestran ser agentes ideales en el biocontrol de plagas de interés agronómico. Su utilización como insecticidas biológicos es impulsada debido a su elevada patogenicidad, su especificidad sobre el insecto blanco, su persistencia en el ambiente y otras características como su fácil aplicación en los cultivos. También, se puede destacar su prolongada viabilidad ante diversas condiciones de almacenamiento.
Los productos comerciales que se utilizan a nivel regional demuestran ser altamente eficientes en el control de plagas presentes en cultivos hortícolas. Estos insumos, dependiendo del número de agentes virales contenidos en el formulado de comercialización, pueden tener una o varias plagas como especie blanco. La posibilidad de combinar en una formulación más de un agente viral es una opción que permite ampliar su espectro insecticida. En este aspecto, también está demostrada la compatibilidad de uso de los baculovirus con otros bioinsecticidas a base de bacterias u hongos entomopatógenos.
Si bien el comercio regional de los baculovirus es relativamente bajo en comparación con otros tipos de bioinsumos aplicados al control de plagas, los datos actuales indican un aumento sostenido de su utilización en los últimos años. Aunque no hay datos precisos sobre el ámbito en el cual son empleados estos bioinsecticidas, los sistemas hortícolas presentan características ideales para su aplicación.
Las economías locales y regionales, centradas básicamente en la producción de alimentos frescos para consumo interno y exportación, son mercados propicios y aún poco explotados para la introducción de bioinsumos como los baculovirus. Ante este escenario, se hace necesaria la difusión de las características de estos insumos entre los productores del sector, así como la implementación de medidas comerciales y regulatorias que alienten su comercialización y empleo. Esto último, podría acelerar la incorporación de estos bioinsecticidas, como herramientas de protección vegetal de bajo impacto, en los sectores de producción hortícola de la región.
BIBLIOGRAFÍA
AFOLAMI, O.; OLADUNMOYE, M. 2017. Baculoviruses: Emerging Frontiers for Viral Biocontrol of Insect Pests of Agricultural Importance. Journal of Advances in Microbiology. 5(4): 1-7.
Arrizubieta, M.; Simón, O.; Torres-Vila, L.M.; Figueiredo, E.; Mendiola, J., Mexia, A.; Caballero, P.; Williams, T. 2016. Insecticidal efficacy and persistence of a co-occluded binary mixture of Helicoverpa armigera nucleopolyhedrovirus (HearNPV) variants in protected and field-grown tomato crops on the Iberian Peninsula. Pest Manag Sci. 72(4): 660-70. doi: 10.1002/ps.4035
BAUTISTA, E.; MESA, L.; GÓMEZ ALVAREZ, M.I. 2018. Alternativas de producción de bioplaguicidas microbianos a base de hongos: el caso de América Latina y El Caribe. Scientia Agropecuaria, 9(4), 585-604. doi.org/10.17268/sci.agropecu.2018.04.15
Behle, R.W.; Tamez-Guerra, P.; McGuire, M.R. 2003. Field activity and storage stability of Anagrapha falcifera nucleopolyhedrovirus (AfMNPV) in spray-dried lignin-based formulations. J Econ Entomol. 96(4):1066-75. doi: 10.1603/0022-0493-96.4.1066
BERRETTA, M.F.; RIOS M.L.; SCIOCCO DE CAP, A. 1998. Characterization of a nuclear polyhedrosis virus of Spodoptera frugiperda from Argentina J Invertebr Pathol 71:280-282. doi:10.1006/jipa.1997.4731
BLISSARD, G.W.: THEILMANN, D.A. 2018. Baculovirus Entry and Egress from Insect Cells Annual review of virology 5:113-139. doi:10.1146/annurev-virology-092917-043356
BOLETÍN DE INFORMACIÓN TÉCNICA GEMSTAR®. 2020. (Disponible: https://www.certisusa.com/pest_management_products/insecticidal_viruses/gemstar_biological_insecticide verificado: junio de 2020).
BOLETÍN DE INFORMACIÓN TÉCNICA HELICOVEX® .2020. (Disponible: https://www.andermattbiocontrol.com/sites/products/bio-insecticides/helicovex.html verificado: junio de 2020).
BOLETÍN DE INFORMACIÓN TÉCNICA LITTOVIR® .2020. (Disponible: https://www.andermattbiocontrol.com/sites/products/bio-insecticides/ littovir.html verificado: junio de 2020).
BOLETÍN DE INFORMACIÓN TÉCNICA LOOPEX® .2020. (Disponible: https://www.andermattbiocontrol.com/sites/products/bio-insecticides/loopex.html verificado: junio de 2020).
BOLETÍN DE INFORMACIÓN TÉCNICA SPEXIT®. 2020. (Disponible: https:// www.andermattbiocontrol.com/sites/products/bio-insecticides/spexit.html verificado: junio de 2020).
BOLETÍN DE INFORMACIÓN TÉCNICA TUTTAVIR®. 2020. (Disponible: https:// www.andermattbiocontrol.com/sites/newsletter-01-2018/tutavir.html verificado: junio de 2020).
BOLETÍN DE INFORMACIÓN TÉCNICA VPN-ULTRA®. 2020. (Dsiponible: http://agricolaelsol.com/vpn-ultra-16-wp/ verificado: junio de 2020).
COUCH, T.L.; IGNOFFO, C.M. 1981. Formulation of insect pathogens. En: BURGES, H.D. (Ed). Microbial Control of Insect Pests and Plant Diseases.; Academic Press, Londres, Reino Unido. 621-634 pp.
CUARTAS-OTALORA, P.E.; GOMEZ-VALDERRAMA, J.A.; RAMOS, A.E.; BARRERA-CUBILLOS, G.P.; VILLAMIZAR-RIVERO, L.F. 2019. Bio-Insecticidal Potential of Nucleopolyhedrovirus and Granulovirus Mixtures to Control the Fall Armyworm Spodoptera frugiperda (J.E. Smith, 1797) (Lepidoptera: Noctuidae). Viruses 11(8), 684 doi:10.3390/v11080684
DADER, B.A.; AGUIRRE, E.; CABALLERO, P.; MEDINA, P. 2020. Synergy of Lepidopteran Nucleopolyhedroviruses AcMNPV and SpliNPV with Insecticides. Insects 11(5), 316. doi:10.3390/insects11050316
DESHAYES, C.S.; PAURON, D.; FROGER, J. A.; LAPIED, B.; APAIRE-MARCHAIS, V. 2017. Microbial Pest Control Agents: Are they a Specific and Safe Tool for Insect Pest Management? Current medicinal chemistry 24:2959-2973. doi:10.2174/0929867324666170314144311
FERRELLI, M.L.; PIDRE, M.L.; GHIRINGHELLI, P.D.; TORRES, S.; FABRE, M.L.; MASSON, T.; CEDOLA, M.T.; SCIOCCO-CAP, A.; ROMANOWSKI, V. 2018. Genomic analysis of an Argentinean isolate of Spodoptera frugiperda granulovirus reveals that various baculoviruses code for Lef-7 proteins with three F-box domains PLoS One 13:e0202598. doi:10.1371/journal.pone.0202598
FERRELLI, M.L.; TAIBO, C.; FICHETTI, P.; SCIOCCO-CAP A.; ARNEODO, J.D. 2016. Characterization of a new Helicoverpa armigera nucleopolyhedrovirus variant causing epizootic on a previously unreported host, Helicoverpa gelotopoeon (Lepidoptera: Noctuidae). J. Invertebr. Pathol. 138:89-93. doi:10.1016/j.jip.2015.08.009
FULLER, E.; ELDERD, B.D.; DWYER, G. 2012. Pathogen persistence in the environment and insect-baculovirus interactions: disease-density thresholds, epidemic burnout, and insect outbreaks. The American naturalist 179: E70-96 doi:10.1086/664488
GLARE, T.R.; GWYNN, R.L.; MORAN-DIEZ, M.E. 2016. Development of Biopesticides and Future Opportunities. Methods Mol Biol. 1477:211-221. doi:10.1007/978-1-4939-6367-6_16
GRANADOS, R.R.; FEDERICI, B.A.1986. The biology of baculoviruses. CRC Press, Boca Raton, Florida.
GRÖNER, A. 1986.Specificity and safety of baculoviruses. En: GRANADOS, R.; FEDERICI, A. (Ed.). The Biology of Baculoviruses. Boca Raton: CRC Press, Vol. 1, 177-202 pp.
GRZYWACZ, D.; MOORE, S. 2017. Production, Formulation, and Bioassay of Baculoviruses for Pest Control. Chapter 7. Microbial control of Insect and Mite Pest, Academy Press, Nueva York 482. 107-124 pp.
HAASE, S.; SCIOCCO-CAP, A.; ROMANOWSKI, V. 2015. Baculovirus Insecticides in Latin America: Historical Overview, Current Status and Future Perspectives Viruses 7:2230-2267.
HAN, G.L.; LIU, Q.; XU, J. 2015. Synergistic Effect of Combining Plutella xylostella Granulovirus and Bacillus thuringiensis at Sublethal Dosages on Controlling of Diamondback Moth (Lepidoptera: Plutellidae). J. Econ. Entomol. 108: 2184-2191. doi:10.1093/jee/tov182
JAKUBOWICZ, V.; TAIBO, C.B.; SCIOCCO-CAP, A.; ARNEODO, J.D. 2019. Biological and molecular characterization of Rachiplusia nu single nucleopolyhedrovirus, a promising biocontrol agent against the South American soybean pest Rachiplusia nu. J Invertebr Pathol. doi: 10.1016/j.jip.2019.107211
JAQUES R.P.; LAING, D.R.; YU, D.S. 1987. Effectiveness and persistance of the granulosis virus of the codling moth Cydia pomonella (L) (Lep: Oleuthreutidae) on apple. Can. Entomol. 119: 1063-1067.
JARVIS, D.L.; GARCIA, A. JR. 1994. Long-term stability of baculoviruses stored under various conditions. Biotechniques 16(3): 508-513.
KELLY, B.J.; KING, L.A.; POSSEE, R.D. 2016. Introduction to Baculovirus Molecular Biology. In Baculovirus and Insect Cell Expression Protocols. Humana Press, Nueva York. 25-50 pp. doi:10.1007/978-1-4939-3043-2_2
LACEY, L. 2016. Microbial Control of Insect and Mite Pests: From Theory to Practice. Academy Press.
LACEY, L.A.; FRUTOS, R.; KAYA, H.K.; VAIL, P. 2001. Insect Pathogens as Biological Control Agents: Do They Have a Future? Biological Control 21:230-248.
LACEY, L.A.; THOMSON, D.; VINCENT, C.; ARTHURS, S. P. 2008a. Codling moth granulovirus: a comprehensive review. Biocontrol Science and Technology,18:7,639-663.
LACEY, L.; SHAPIRO-ILAN, D.; FRUTOS, R.; BROWNBRIDGE, M.; GOETTEL, M. S. 2015. Insect pathogens as biological control agents: Back to the future J Invertebr Pathol. 132:1-41. doi:10.1016/j.jip.2015.07.009
LACEY, L.A.; HEADRICK, H.L.; ARTHURS, S.P. 2008b. Effect of temperature on long-term storage of codling moth granulovirus formulations. Journal of Economic Entomology, 101(2), 288-294.
Lasa, R.; Pagola, I.; ibañez, I; Belda, J.E.; Williams, T.; Caballero, P. 2007. Efficacy of Spodoptera exigua multiple nucleopolyhedrovirus as a biological insecticide for beet armyworm control in greenhouses of southern Spain, Biocontrol Science and Technology, 17:3, 221-232. DOI: 10.1080/09583150701211335.
LEGUIZAMÓN, E.S. 2018. Historia de la horticultura. Ediciones INTA. Buenos Aires. (Disponible: https://intagobar/sites/default/files/inta_asaho_historia_horticulturapdf verificado: junio de 2020).
MASCARIN, G.M.; LOPES, R.B.; DELALIBERA, I.; FERNANDES, E.K; LUZ, C.; FARIA, M. 2019. Current status and perspectives of fungal entomopathogens used for microbial control of arthropod pests in Brazil J Invertebr Pathol 165:46-53. doi:10.1016/j.jip.2018.01.001
MISHRA, J.; TEWARI, S.; SINGH, S.; ARORA, N.K. 2015. Biopesticides: Where We Stand? Plant Microbes Symbiosis: Applied Facets Springer India. 37-75 pp.
MOSCARDI, F.; SOSA-GÓMEZ, D.R. 1992. Use of viruses against soybean caterpillars in Brazil. En: COPPING, L.G.; GREEN, M.B.; REES, R.T. (ed.). Pest Management in Soybean. Elsevier Applied Science, Londres, Reino Unido. 98-109 pp.
MURILLO, R.M.; RUÍZ-PORTERO, M.; ALCÁZAR, M.D.; BELDA, J.E.; WILLIAMS, T.; CABALLERO, P. 2007. Abundance and genetic structure of nucleopolyhedrovirus populations in greenhouse substrate reservoirs. Biological Control 42:216-225. doi.org/10.1016/j.biocontrol.2007.04.015
NIZ, J.; SALVADOR, R.; FERRELLI, M.L; SCIOCCO DE CAP, A.; ROMANOWSKI, V.; BERRETTA, M.F. 2020. Genetic variants in Argentinean isolates of Spodoptera frugiperda Multiple Nucleopolyhedrovirus Virus Genes 1-5. doi.org/10.1007/s11262-020-01741-9
PAULI, G.; MOURA MASCARIN, G.; EILENBERG, J.; DELALIBERA, J.I. 2018. Within-Host Competition between Two Entomopathogenic Fungi and a Granulovirus in Diatraea saccharalis (Lepidoptera: Crambidae). Insects 9(2):64. doi:103390/insects9020064
PELAEZ, V.; MIZUKAWA G. 2017. Diversification strategies in the pesticide industry: from seeds to biopesticides Estratégias de diversificação na indústria de agrotóxicos: de sementes a biopesticidas. Ciência Rural 47(2): 1-7.
PIDRE, M.; SABALETTE, S.; ROMANOWSKI, V.; FERRELLI, M.L. 2019. Identification of an Argentinean isolate of Spodoptera frugiperda granulovirus. Rev. Argent. Microbiol. 51(4), 381-385. doi:10.1016/j.ram.2018.10.003
QUINTANA, G.; ALVARADO, L. 2004. Carpovirus Plus: Primer insecticida biológico para el control de Cydia pomonella en montes comerciales de pera, manzana y nogal. AgroInnova La Innovación Tecnológica para Mejorar la Competitividad; SECyT-INTA: Rosario, Argentina. 15-17 pp.
RODRÍGUEZ, V.; BELAICH, M.; QUINTANA, G.; SCIOCCO-CAP, A.; GHIRINGHELLI, P.D. 2012. Isolation and Characterization of a Nucleopolyhedrovirus from Rachiplusia nu (Guenée) (Lepidoptera: Noctuidae). Int J Virol. Mol. Biol. 1, 28-34.
ROHRMANN, G.F. 2019. Baculovirus Molecular Biology [Internet]. 4th ed. Bethesda (MD): National Center for Biotechnology Information (US). PMID: 31294936.
TAMEZ-GUERRA, P.; MCGUIRE, M.R.; BEHLE, R.W.; SHASHA, B.S; PINGEL, R.L. 2002. Storage stability of Anagrapha falcifera nucleopolyhedrovirus in spray-dried formulations J Invertebr Pathol. 79:7-16. doi:10.1016/S0022-2011(02)00005-8
THEILMANN, D.A.; BLISSARD, G.W.; BONNING, B.; JEHLE, J.A.; O’REILLY, D.R.; ROHRMANN, G.F.; THIEM, S.; VLAK, J.M. 2005. Baculoviridae. En: FAUQUET, C.X.; MAYO, M.A.; MANILOFF, J.; DESSELBERGER, U.; BALL, L.A. (eds.). Virus Taxonomy—Classification and Nomenclature of Viruses. 8th Report of the International Committee on the Taxonomy of Viruses. Elsevie Ámsterdam. 177-185 pp.
Valicente, F.H.; da Costa, E.F.1995. Controle da lagarta do cartucho Spodoptera frugiperda (J.E. Smith) com Baculovirus spodoptera, aplicado via agua de irrigação. An. Soc. Entomol. Brasi. 24, 61-67.
