Resumen: Se detallan experimentos de química y de física, contextualizados en el ámbito de la realización de efectos especiales en cine y teatro. El objetivo principal, aparte de mostrar los resultados de una labor desarrollada, es ofrecer ideas a profesores y divulgadores científicos para sus actividades. A través de aplicaciones concretas, vistosas e interesantes para alumnos y público en general, se muestran y discuten conceptos como: reacciones químicas, termoquímica, cristalización, densidad, índice de refracción, hidratación, sublimación, condensación, plásticos higroscópicos, pigmentos termocrómicos y seguridad en la experimentación científica, entre otros.
Palabras clave:Actividades recreativasActividades recreativas, Aprendizaje por descubrimiento Aprendizaje por descubrimiento, Cine Cine, Divulgación Divulgación, Experimentación Experimentación, Física Física, Química Química.
Abstract: In this paper, experiments in chemistry and physics are described, contextualized in the field of performing special effects in filmmaking and theatre. Besides showing the work we have developed, our aim is offering ideas to teachers and science communicators for their activities. A wide variety of concepts such as chemical reactions, thermo-chemistry, crystallization, density, refractive index, hydration, sublimation, condensation, hygroscopic plastics, thermo-chromic pigments and safety guidelines for science experiments are shown and discussed, all this through the achievement of engaging and interesting activities for students and general public.
Keywords: Recreational Activities, Discovery Learning, Filmmaking, Science outreach, Experimentation, Physics, Chemistry.
Ciencia recreativa
Química y física de algunos efectos especiales en cinematografía: Una propuesta educativa y para la divulgación
Chemistry and physics of some special effects in filmmaking: An educative and for public outreach proposal
Universidad de Cádiz

Esta obra está bajo una Licencia Creative Commons Atribución-NoComercial-SinDerivar 4.0 Internacional.
Recepción: 01 Diciembre 2016
Aprobación: 01 Febrero 2017
Como se ha señalado en anteriores trabajos, una de las estrategias educativas más recurrentes para la enseñanza de las ciencias experimentales, es el empleo de ejemplos contextualizados, (Prolongo et al. 2014). Esto supone un factor de motivación importante para los alumnos, dado que perciben así la necesidad de aprender conceptos y contenidos para interpretar y comprender aspectos relacionados con su experiencia personal. Por otra parte, es indudable el creciente interés que, en los últimos años, están teniendo los eventos y las actividades de divulgación y difusión de la ciencia, mediante, por ejemplo, la exposición de experiencias prácticas destinadas a un público variado (Pinto et al. 2014).
Existe un gran número de referencias sobre ciencia recreativa. Entre otros trabajos al respecto se pueden citar algunos de los aparecidos en el monográfico que esta publicación dedicó al tema hace unos años (Corominas 2011, García Liarte y Peña Martínez 2011, García-Molina 2011, Gómez Crespo y Cañamero Lancha 2011, Vega Palas 2011), así como, ya más centradas en la química, algunas recopilaciones sobre experiencias curiosas para enseñar y divulgar esta ciencia (Aguilar Muñoz et al. 2011, Alonso Felipe 2016, Roesky y Möckel 1996).
En este trabajo presentamos la propuesta de un conjunto de actividades prácticas con potencial interés para los dos ámbitos aludidos, el educativo y, de forma especial, el divulgativo. Son experiencias especialmente dirigidas a muestras recreativas y divulgativas, aplicables en un entorno tanto escolar como extraescolar, y que consisten en experimentos de química y de física, adaptables tanto al público en general como a estudiantes de las diferentes etapas educativas, en torno a los efectos especiales utilizados en cinematografía.
El uso de recursos relacionados con el ámbito del cine para abordar aspectos científicos en el aula ha sido objeto de diversas propuestas (Diener 2010, Griep y Mikasen 2009). El trabajo que se presenta aquí, más que en películas o escenas concretas, como las referencias citadas, se centra en las aportaciones de la química y la física para generar los efectos especiales propios del rodaje cinematográfico y del teatro.
A través de experiencias y demostraciones, se abordan aspectos educativos y divulgativos sobre una gran variedad de conceptos (reacciones ácido-base, redox y de formación de complejos, termoquímica, indicadores ácido-base, cristalización de sales, densidad, índice de refracción, hidratación, sublimación, condensación, coloides, formulación, plásticos higroscópicos, pigmentos termocrómicos y otros), a la vez que se intenta plasmar cómo la química y la física encuentran multitud de aplicaciones prácticas a problemas concretos.
Se ha incluido un apartado específico sobre precauciones y recomendaciones de procedimiento, dado que la seguridad y prevención de riesgos es de vital importancia en este tipo de actividades. En todo caso, se entiende que la publicación se dirige a profesionales especializados, docentes y divulgadores, que son conscientes de la necesidad de velar por todo ello. Así, algunas de las fotografías que se recogen en este trabajo son ilustrativas de la actividad, pero no del procedimiento seguido exactamente en la práctica que, por ejemplo, puede conllevar la utilización de gafas de seguridad o una vitrina de gases.
Estas experiencias se han llevado a la práctica, de forma separada, en distintas etapas educativas (desde Educación Secundaria Obligatoria a primer curso universitario), obviamente con los matices pertinentes para adecuarlas al nivel de los alumnos y el temario impartido en el momento. También se han realizado, de manera conjunta, en forma de taller de entre 30 y 45 minutos de duración. Como ejemplo de esto último, se impartieron varios talleres para el público en general, en octubre de 2016 en el certamen de Ciencia en Acción celebrado en Algeciras (Cádiz).
Una revisión sobre los efectos especiales principales en cinematografía y su relación con la química se puede encontrar en un reciente trabajo (Muñoz-Osuna et al. 2013), donde se recopilan además interesantes referencias.
De acuerdo al diccionario de la Real Academia Española, los efectos especiales son «la técnica de algunos espectáculos, trucos o artificios para provocar determinadas impresiones que producen ilusión de realidad». En un ámbito general, se suelen dividir en varios tipos: ópticos (visuales o fotográficos), mediante manipulación de imágenes fotografiadas; mecánicos (prácticos o físicos), realizados durante el rodaje en vivo de una película; de sonido (o de audio); de maquillaje y digitales.
Aunque la química es esencial en otros tipos de efectos especiales, como los de maquillaje, en este trabajo nos referiremos esencialmente a los denominados mecánicos, donde se suelen incluir efectos ambientales, sangre artificial, caracterización, pirotecnia, disparos, explosiones, niebla, bruma y humo, entre otros. En todo caso, en las demostraciones que se sugieren en los siguientes apartados, prescindiremos de las relacionadas con explosiones, efectos pirotécnicos y preparación de humos de distintos colores, pues se han abordado en otros trabajos (de Prada 2006, de Prada 2013, Pinto y Vieta 2013).
Los objetivos que se pretenden con el conjunto de experiencias recogidas en este artículo son:
- Facilitar el aprendizaje de conceptos químicos y físicos.
- Promover la curiosidad y la indagación.
- Favorecer el razonamiento crítico.
- Mostrar la necesidad de experimentar para aprender ciencia.
- Fomentar la cultura científica entre estudiantes y público en general.
- Indicar ejemplos que ayuden a apreciar algunas aplicaciones de la química y de la física.
De alguna manera, el objetivo principal es que, a través de aplicaciones concretas propias del mundo de los efectos especiales, y del cine en general, los participantes se den cuenta y perciban que, gracias a la ciencia, se consigue una mejor calidad de vida. Hablando de cinematografía, esta idea la resume el título (aunque el argumento va por otros derroteros) de la película Better living through chemistry, estrenada en 2014 y que en español se tradujo como La fórmula de la felicidad. En el propio cartel del anuncio de la película (ver figura 1) se alude a instrumentos típicos del laboratorio y a ejemplos de formulación (con erratas incluidas).

Figura 1.
Cartel de una película cuyo título resume el mensaje principal que se pretende transmitir con las actividades propuestas y otras análogas.
Tanto como propuesta educativa como de ejemplo de actividad divulgadora, la presentación de las actividades se presentan como respuesta experimental a preguntas que se hacen previamente. Por ello, se muestra aquí una recopilación de preguntas típicas que se plantean a alumnos o participantes para, seguidamente, responderlas a través de las experiencias propuestas. Con ello se pretende favorecer la indagación y la observación.
Entre otras preguntas, y aparte de las que normalmente surgen cuando los participantes van aportando respuestas (es frecuente que la respuesta a un fenómeno abra nuevos interrogantes), se destacan las siguientes:
- ¿Por qué se denomina «hielo seco» a una sustancia comercial? ¿Qué es? ¿Por qué se hunde en agua? En contacto con agua: ¿se forma humo o niebla? ¿Por qué no asciende como otros gases? ¿Por qué cambia de color una disolución de indicador ácido-base en agua al añadir hielo seco?
- ¿Cómo se prepara la nieve artificial para filmación de películas?
- ¿Cómo se simula la sangre producida por cortaduras ficticias en el cine y en el teatro?
- ¿Se puede preparar una niebla que salga de forma violenta de una botella o «lámpara tipo árabe», como si fuera un «genio», al abrirla?
- ¿Se puede usar una reacción química para simular una erupción volcánica en una maqueta?
- ¿Hay alguna reacción química que se usara para generar la luz de los flashes en los orígenes de la fotografía?
- ¿Qué es la kryptonita de las películas de Supermán? ¿Podemos preparar fácilmente algo parecido?
- ¿Podemos hacer un objeto invisible al sumergirlo en un líquido?
- ¿Cómo se puede preparar una tinta invisible como la utilizada por los espías en las películas?
- ¿Se puede simular una cerveza de forma rápida?
Con las experiencias que se exponen se pretende que los participantes respondan a las preguntas planteadas anteriormente. La mayor parte de los experimentos se pueden realizar en un aula o en una sala típica de ferias científicas o exposiciones, sin ser imprescindible el uso del laboratorio. En algún caso, será necesario el laboratorio para operar en vitrina de gases.
La mayor parte son experiencias clásicas de física y de química. Algunas de ellas ya se detallaron por los autores en otros trabajos (Alonso Felipe 2016, Pinto y Prolongo 2012). En todo caso, se destacan como aportaciones principales, aparte de la recopilación en torno a un tema atrayente para el público en general (los efectos especiales), la formulación de observaciones adicionales, la discusión mediante preguntas e indagaciones, y la profundización en la explicación científica, tratando de huir del mero efecto sorpresa.
Muchos de los efectos especiales presentados se pueden preparar de distintas formas, con procesos químicos o físicos alternativos. Como ya se ha indicado, el objetivo del trabajo es de tipo educativo y no de carácter recopilatorio.
Aunque es un compuesto que suele ser conocido por programas de televisión y muestras en ferias científicas, tanto los alumnos como el público en general suelen desconocer qué es exactamente el conocido como «hielo seco». En este sentido, se sugiere introducirlo mostrando su aspecto y discutiendo por qué se denomina así: parece hielo común pero no funde formando agua, como éste, sino que pasa a gas directamente. El hecho de que pase a gas se visualiza porque cada vez es más pequeño el sólido y se forma una «neblina». Es interesante destacar cómo los participantes pueden visualizar un proceso físico, la sublimación, que en los libros de texto se suele ejemplarizar casi únicamente con sustancias antipolilla como el naftaleno (popularmente conocido como «naftalina»).
Es típico que en el grupo que participa en la actividad alguien destaque que se trata de «nitrógeno líquido». La confusión se debe a que a través de la televisión se han popularizado experimentos tanto con hielo seco como con nitrógeno líquido. Tras resaltar que se ve a simple vista que no se trata de un líquido, se especifica que se trata de CO2 sólido. Se puede aprovechar para resaltar que, aparte de dióxido de carbono, se conoce también, incluso a nivel comercial (el público lo puede leer en la propia caja que lo contiene) como anhídrido carbónico, según una nomenclatura química hoy en desuso. El CO2 es de los compuestos más conocidos por el público no especializado, por las alusiones frecuentes en medios de comunicación al denominado efecto invernadero o calentamiento global que contribuye a provocar, y por su presencia en las bebidas gaseosas.
Para resaltar hasta qué punto puede llegar la discusión con el público en función de las observaciones, cuando se expone la experiencia a niños, de lo que más les llama la atención es que la caja que lo contiene (de poliexpán con paredes gruesas) les recuerda a las que conocen para transportar helados o para mantener bebidas frías en el campo y en la playa.
Inicialmente, se informa de su composición y del hecho de que se puede adquirir fácilmente a nivel particular (hay empresas que lo dispensan vía online, por ejemplo para ambientar fiestas como cumpleaños o de Halloween y para preparar bebidas «sofisticadas»). En todo caso, se recalca que deben cumplirse las precauciones indicadas por el fabricante y por el distribuidor. Entre las instrucciones de manipulación y características del producto señaladas en la etiqueta, se destaca que se encuentra a unos –80 ºC. Para la experiencia que se recoge aquí se recomienda trabajar con hielo seco en forma de pellets. Para tener el menor contacto físico con esta sustancia se sugiere el empleo de algún utensilio, como una cuchara. Para su correcta manipulación, se recomienda la lectura de la ficha de datos de seguridad (FDS) del hielo seco (Linde 2015).
Seguidamente, se anuncia a los participantes que observen qué ocurre cuando se vierte hielo seco en agua, así como en agua con unas gotas de indicador ácido-base. Un indicador típico para esto es el azul de bromotimol, que es azul en medio acuoso ligeramente básico (se puede intensificar el color añadiendo unas gotas de disolución de NaOH) y se colorea a amarillo en medio ácido. Su intervalo de viraje está entre valores de pH de 6,0 y 7,6. Para favorecer la observación, se puede indicar que se fijen en el hecho de si su hunde o no (caso del hielo común, que flota en agua), si se modifica el color, y si se aprecia algún otro cambio.
Al echarlo en agua, ante la sorpresa general por todo lo que ocurre en un instante, se observa que se hunde (es más denso que el agua), pasa directamente a gas, formando grandes burbujas y, con el indicador señalado, pasa de color azul a amarillo, como se aprecia en la figura 2.
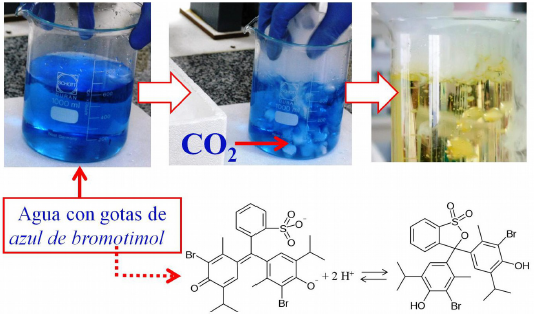
Figura 2.
Resultado de la experiencia de añadir hielo sexo en disolución acuosa ligeramente básica con unas gotas de indicador azul de bromotimol, del que se incluye su estructura molecular (en función del pH).
Se demuestra así el carácter ácido de la disolución carbonatada, con lo que se puede, además, introducir el fundamento de las bebidas carbónicas. También se forma una niebla que sorprende porque se queda abajo, y que precisamente es la que sirve para generar ambientes misteriosos y de terror, tanto en cine como en teatro. Esto se explica por la mayor densidad del CO2 frente al aire (por eso se usa este compuesto en extintores de incendio).
El frío que se produce en el medio acuoso al añadir hielo seco se puede ilustrar con envases y objetos de plásticos termocrómicos (poseen pigmentos que cambian de color al variar la temperatura), como se muestra en la figura 3. Estos se consiguen con cierta facilidad en museos de ciencia, tiendas especializadas de juegos científicos o como juguetes que de vez en cuando se ofrecen con los menús de niños en cadenas de comida rápida como hamburgueserías (como es el caso de la figura señalada). Es un ejemplo interesante de materiales específicos, desarrollados gracias a la química.

Figura 3.
Cambio de color producido al enfriarse un envase termocrómico, inicialmente rosa a unos 22 ºC, y en una pajita (también termocrómica) que al principio era blanca, al estar en contacto con agua sobre la que se añadió hielo seco. En el caso de la pajita, se debe sorber el agua con aspirador manual para pipetas, para evitar riesgos.
Se trata de una experiencia que ofrece muchos recursos educativos y para la discusión. Es frecuente que, si se añade bastante cantidad de hielo seco, se observe en el fondo un sólido blanquecino que asciende hasta la superficie del agua: se debe a la formación, a baja temperatura, de hielo (agua sólida) que sube por su menor densidad. Otro efecto que se suele observar es la condensación de agua en la parte exterior del recipiente, al descender la temperatura por el hielo seco añadido. Si se pregunta a los participantes de dónde procede esa agua, no es raro encontrar respuestas del tipo: «sale del recipiente, atravesando los poros».
También pude especificarse con esta actividad la diferencia entre humo (que es lo que muchos participantes dicen que ven) y niebla; ambos son coloides, pero en el primer caso se trata de partículas sólidas en el aire y, en el segundo, de gotitas de líquido (agua) dispersas en el aire. La niebla se hace más intensa si se opera con agua caliente. Como ejemplo de que este tipo de experiencias pueden dar lugar a profundizar en conceptos, se recomienda un reciente trabajo (Kuntzleman et al. 2015) donde se prueba que, contrariamente a lo pensado por la mayor parte de profesores y divulgadores, las gotitas que forma la niebla al añadir hielo seco en agua proceden principalmente del líquido, y no de la condensación del vapor de agua atmosférico. Esto muestra que hechos divulgativos cotidianos y bien conocidos pueden tener cierta complejidad en su interpretación.
Aunque se prepara también de otros modos (Muñoz-Osuna et al. 2013), una forma de preparación de nieve artificial en el rodaje de películas es mediante un polímero superabsorbente de agua, como el poliacrilato de sodio. La experiencia que se sugiere puede servir para discutir la ley de conservación de la masa y para observar que se absorbe gran cantidad de agua por parte de este material, usado en la fabricación de pañales, como ya se explicó en un anterior trabajo (Pinto y Prolongo 2012). En este caso se sugiere introducir el tema mediante un «truco de magia» para llamar la atención de los participantes, especialmente si son niños. Inicialmente se disuelve el contenido de un sobre de azúcar con media copa de agua. Al repetir lo mismo con un sobre «trucado» (contiene el polímero superabsorbente en vez de azúcar), por ejemplo al tocarlo con una «varita mágica» se forma gran cantidad de sólido con aspecto de nieve (ver figura 4). Incluso al tacto, el material tiene aspecto de «nieve» y está algo frío (por la evaporación del agua).
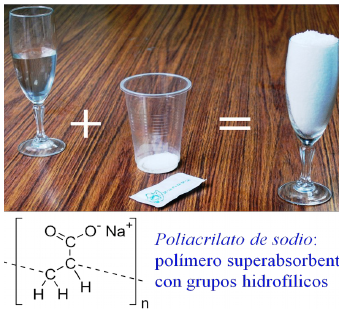
Figura 4.
Ilustración del experimento propuesto para mostrar la formación de nieve artificial (explicación detallada en el texto), mediante un truco de magia, y la estructura del poliacrilato de sodio.
Sobre una mano, protegida con una película de plástico o con un guante de goma, para mayor seguridad, se deposita con pincel una disolución de tiocianato de amonio o de potasio; al pasar por encima un cuchillo de plástico o una espada de juguete, mojados en disolución de cloruro de hierro(III), se forma el ion complejo [Fe(SCN)(H2O)5]2+ de color rojo con aspecto de sangre (ver figura 5).
Es uno de los procedimientos que se sigue en el cine para simular la formación de sangre por «cortadoras» ficticias. Incluso se ha sugerido que este tipo de reacción pudo haberse utilizado en el rodaje de una escena emblemática de la película Los diez mandamientos, dirigida y producida por Cecil B. DeMille en 1956, en la que el agua del Nilo se transforma en sangre al tocarla Charlton Heston (en el papel de Moisés) con su vara (López Pérez y Boronat Gil 2012).
La reacción simplificada, que explica la obtención del pentaacuo-(tiocianato-N)hierro(III) es:
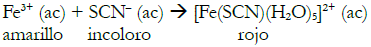 (1)
(1)
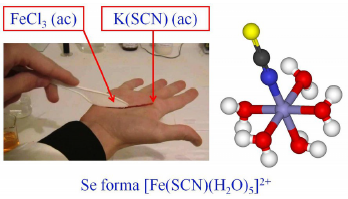
Figura 5.
Preparación de sangre artificial y estructura del complejo formado. Para evitar el contacto con la piel, se dispuso una capa de plástico invisible sobre la mano al realizar la fotografía.
En una botella opaca se introduce disolución acuosa de agua oxigenada (30 % p/v). En el tapón (de corcho) se adhiere con hilo un trozo de papel formando un paquete que contiene permanganato de potasio. Al abrir la botella cae el paquete al interior de la botella, produciéndose una rápida emisión de niebla: se debe a una reacción redox en la que se forma oxígeno y agua. Al condensar (y proyectarse desde la disolución) parte del agua en forma de gotitas, se genera la niebla (figura 6), como la que aparece en las películas al salir el «genio» de una «lámpara maravillosa». Para una mayor seguridad en su manipulación, se incluye información sobre la FDS de la disolución de H2O2 utilizada (Labbox Labware 2015).

Figura 6.
Ilustración de la reacción redox que produce el efecto de un «genio» saliendo de una botella. Aunque la profesora que realizó el proceso no lleva protección en los ojos, se debe a que la fotografía se tomó extremando las precauciones. Debe procederse siempre con gafas de seguridad.
La reacción química que explica el fenómeno es:
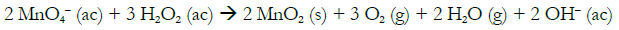 (2)
(2)Si los participantes tocan el fondo de la botella al final, aprecian que se ha calentado. Es una ocasión para explicar que hay reacciones exotérmicas y endotérmicas.
Aunque las maquetas para el rodaje cinematográfico se emplean cada vez menos, dado que se sustituyen por efectos especiales virtuales realizados con medios informáticos, han sido muy importantes en la historia del cine. En este sentido, una experiencia química clásica, que sirve de introducción a este aspecto es la generación de reacciones redox que emiten gran cantidad de gases en procesos exotérmicos. Hay varias, una de ellas es la descomposición del dicromato de amonio (figura 7) según la reacción:
 (3)
(3)Para que se inicie esta reacción se suele utilizar una mecha de magnesio. Por otra parte, la observación de la emisión de luz blanca de alta intensidad por parte de este metal, al reaccionar con oxígeno del aire para dar óxido de magnesio, sirve para ilustrar el empleo de los primeros flashes en fotografía, que contenían polvo de magnesio. Esta reacción de combustión, que necesita un aporte de calor (normalmente con llama de mechero) para que se inicie, se puede describir con la ecuación química:
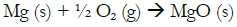 (4)
(4)

Figura 7.
Maqueta de volcán realizada por uno de los autores (J.V.A.) y «erupción» provocada por la reacción redox discutida en el texto. Esta experiencia se lleva a cabo en vitrina de gases de laboratorio.
Si se observa detenidamente cuando se produce, se aprecia perfectamente cómo el magnesio, con aspecto metálico, se transforma en un compuesto blanco (óxido de magnesio). Esto puede servir, junto con otras experiencias, para que los participantes discutan si se está observando una reacción química o un proceso físico. Para facilitar esta reacción es necesario limar previamente la superficie de la cinta de magnesio, para eliminar la capa de óxido exterior, así como cortar en flecos la punta donde se va a aplicar la llama de mechero.
Si no se muestra el volcán y se quiere realizar solo la demostración de la emisión de luz del magnesio, ya de por sí bastante espectacular, se puede hacer con cable de este metal en vez de cinta.
La cristalización de dihidrogenofos-fato de amonio en forma de grandes cristales verdosos puntiagudos se puede usar para introducir otros aspectos de cinematografía. Estos cristales espectaculares, que se forman con cierta facilidad por procesos de recristalización de fertilizantes comerciales (Durán Torres y Martínez Martín 2012, Prolongo 2012), son muy similares a la kryptonita, como se aprecia en la figura 8. La kryptonita es el mineral ficticio que aparece en los cómics y películas de Supermán, «generado» en Kryptón (el planeta natal de este personaje de ficción) y que «anula» sus poderes. Aparte de la cuestión de los cristales, también se puede emplear este ejemplo para explicar a los participantes cómo hay películas donde se usa vocabulario científico o pseudocientífico para aspectos irreales. Así, el nombre de Kriptón se corresponde realmente con el nombre de un elemento químico (Kr), de la familia de los gases nobles, cuya denominación (como el término más conocido, criptografía) proviene del adjetivo griego κρυπτóν (oculto).

Figura 8.
Cristales preparados por alumnos del I.E.S. Manuel Romero (Villanueva de la Concepción, Málaga) y comparación con la kryptonita de Supermán.
Estos cristales se han popularizado entre muchos alumnos de educación secundaria a raíz de concursos, como el de «Cristalización en la Escuela», que se inició en 2014 con motivo del Año Internacional de la Cristalografía.
En un bote transparente con agua (preferentemente destilada) se introduce (unos dos días antes de su exposición) una bola (entre 0,5 cm y 1,0 cm de diámetro) de poliacrilato sódico comercial (mismo compuesto que el de la experiencia de la nieve artificial, pero en distinta forma física). Al hincharse totalmente por absorción de gran cantidad de agua no se ve. Se debe a que posee el mismo índice de refracción que el agua y así, no se produce refracción ni reflexión de la luz. Pero si se vierte, poniendo la mano, se observa una gran bola transparente (similar a las de vidrio de los «adivinos») que, además, permite discutir algunos efectos ópticos, como la inversión de la imagen. Esta experiencia, que es una de las más espectaculares entre los participantes, que no entienden cómo ha aparecido la bola, se ilustra en la figura. 9. Otras aplicaciones lúdicas de los polímeros superabsorbentes fueron tratadas por Gómez Crespo y Cañamero Lancha (2011).

Figura 9.
Aspecto del bote con la esfera de poliacrilato de sodio hidratado (indistinguible si está sumergida en agua) y niños observando con asombro cómo aparece la bola al retirar el agua.
Otro ejemplo de «invisibilidad», típico de películas de espías, es el uso de tintas que se hacen invisibles o no al rociarse con un líquido determinado. Un ejemplo ilustrativo consiste en escribir con una disolución de ácido clorhídrico diluido en la que se añaden unas gotas de fenolftaleína (indicador ácido-base incoloro en medio ácido y neutro, y fucsia en medio básico, con intervalo de viraje de pH entre 8,2 y 10,0). Al añadir (por ejemplo con espray) una disolución de NaOH diluido se visualiza lo escrito. Si seguidamente se rocía con la disolución de HCl el mensaje vuelve a «desaparecer». Un ejemplo de disposición de envases para esta experiencia se muestra en la figura 10.

Figura 10.
Materiales necesarios para preparar un tipo de tinta invisible y para provocar su visibilidad.
Como en otros casos de lo expuesto en este trabajo, si anteriormente se ha realizado ante los participantes la experiencia 1 y se ha hablado de los indicadores ácido-base, en esta experiencia se puede preguntar inicialmente si alguien ha visto alguna vez alguna sustancia de este tipo. Se refuerza de este modo el sentido pedagógico de las actividades.
Para introducir las sustancias empleadas, disoluciones de HCl y de NaOH, se pueden disponer de dos botellas comerciales (accesi-bles en droguerías y supermercados) de agua fuerte y de desatascador de tuberías, respectiva-mente. Incluso si no se tienen accesibles envases pulverizadores, se puede realizar para ilustrar todo esto un «truco» de magia: con un vaso de plástico en el que se añade con anterioridad unas gotas de disolución de fenolftaleína y se deja evaporar el disolvente, se pregunta a los participantes ¿qué hay en el vaso? Si responden que «nada» se puede responder ¿al menos aire, no? Así, se continúa preguntando qué ocurrirá si sobre ese vaso se añade un poco de «desatascador»; cuando casi todo el mundo piensa que no sucede nada, se transforma en un líquido de color fucsia intenso, ante el asombro general. Con un poco de «agua fuerte» desparece el color de nuevo y además, al tacto con el vaso se observa que es una reacción (la neutralización de la base con el ácido) exotérmica, como otras de experiencias ya comentadas.
En un recipiente (queda más interesante si es una jarrita como las típicas para servir cerveza) se añade una cantidad de disolución acuosa de agua oxigenada (30 % p/v) (Labbox Labware 2015), unas gotas de agua con detergente (por ejemplo de lavavajillas) y una cantidad de disolución acuosa de KI al 0,5 % p/p. Se aprecia la formación inmediata de color amarillo, similar al de la cerveza, y de burbujas que forman una espuma. Se ha producido por la descomposición del agua oxigenada (en H2O y O2) catalizada con KI:
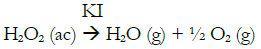 (5)
(5)Parte del yoduro (I–) pasa a yodo (I2), lo que produce la tonalidad amarillenta. Incluso a veces, según las cantidades, se forma el anión triyoduro, I3–, que da una tonalidad más marrón. En este caso, se puede decir que se ha «fabricado» una cerveza morena.
El experimento y el aspecto de la «cerveza» obtenida se ilustran en la figura 11. Más que un recurso cinematográfico, en este caso se trata de una actividad de ilusionismo, área frecuente en películas.

Figura 11.
Ilustración de la fabricación de cerveza artificial según el proceso redox explicado en el texto.
Finalmente, una vez respondidas las respuestas a las preguntas planteadas en cada experiencia, mediante la realización de reacciones químicas o procesos físicos, se puede incidir en la importancia de la química en el propio origen de la fotografía y del cine, con vocabulario como celuloide, filme, película, revelador, sales de plata, fotoquímica, etc. Para ello, se puede mostrar al auditorio (especialmente para el público más joven, que ha crecido con la fotografía digital) un carrete de fotos y comentar brevemente el proceso fotográfico.
Como para tantas reacciones químicas y procesos físicos, debe procederse sin miedo, pero con la adecuada precaución. Por ejemplo, y como ya se ha indicado, no conviene que la «sangre artificial» se haga en la piel de los participantes, por si tuvieran algún tipo de alergia. Para las reacciones químicas, especialmente las exotérmicas y aquéllas en las que hay proyecciones de líquidos o gases, se recomienda que los participantes se coloquen a una distancia prudencial. En algún caso, solo se deberían hacer en vitrina de gases (por ejemplo en visitas de grupos al laboratorio). Además, debe indicarse que no se deben tocar ni las sustancias de partida ni las formadas en las reacciones, salvo excepciones (como la «nieve artificial» obtenida, que puede tocarse sin problema). Tampoco pueden comerse ni llevarse a la boca las sustancias obtenidas (en este caso es especialmente importante porque puede haber público que piense que la cerveza artificial fabricada se puede beber).
Para una correcta manipulación de los reactivos químicos, se recomienda la consulta de su correspondiente ficha de datos de seguridad (FDS), algunas de las cuales se recogen en las referencias.
Otra sugerencia, especialmente si se pretende mostrar este conjunto de experiencias o similares, es el empleo de envases de plástico, como vasos de distinto tamaño, en vez de material de vidrio. Así se facilita el transporte y se evitan roturas.
También se sugiere que se ponga especial empeño en tener todo ordenado y seguir una secuencia de experiencias lógica y de acuerdo con lo que se pretenda mostrar.
Otra recomendación importante, típica de acciones de divulgación, es que se ensayen los reactivos, para tener la certeza de que actuarán según lo previsto. Obviamente no se puede garantizar todo al 100 %, pero el público participante puede quedar decepcionado si espera una reacción vistosa y no se aprecia absolutamente nada. Siempre queda un último recurso, pero no agrada a todo el mundo, y que consiste en decir: aunque no se ha visto ningún cambio, a nivel molecular se han sucedido cambios espectaculares.
Un aspecto fundamental es el de la rigurosidad, así como la atención al nivel formativo de los participantes. Obviamente, no se puede hablar a niños que cursan educación primaria sobre reacciones de formación de complejos, pero sí de lo que es una reacción química, y a alumnos universitarios se les puede comentar en qué consiste una formación de complejos. Todo esto no está reñido con el buen humor y el intento de crear un ambiente de empatía, no solo por el momento sino porque si se muestran aspectos agradables y sorprendentes de la ciencia, el objetivo de divulgación está asegurado.
Suele ser positivo, si se realizan actividades divulgativas por donde pasará mucha gente en poco tiempo, que se pongan paneles explicativos, que puedan servir a los distintos participantes según su nivel formativo y de interés. Esos paneles pueden ser la base de la elaboración de folletos, por si alguien quiere ver todo con más reposo y detalle más adelante. Si además se indica en el folleto la dirección de correo electrónico del profesor o divulgador, se promueve el intercambio de información posterior.
Algunos materiales empleados en estas experiencias se pueden encontrar en supermercados o son habituales en laboratorios de física y química de centros educativos. Para las experiencias 1, 2 y 7 hacen falta objetos termocrómicos (por ejemplo tazas), nieve artificial y bolas de poliacrilato de sodio que no son fácilmente accesibles. Pero existen distribuidores que los ofrecen, junto con otros materiales curiosos para la docencia y la divulgación, como son Ventus Ciencia Experimental ( http://www.ventusciencia.com ) y Educational Innovations ( http://www.teachersource.com ).
Como se indicó en los objetivos planteados, dos importantes son la posibilidad de facilitar el aprendizaje de conceptos implicados en cada experiencia y favorecer el pensamiento crítico. En este sentido, se considera que es cada profesor (o divulgador) particular quien, conociendo con profundidad la experiencia, debe adecuar su realización y exposición a los objetivos que plantee y al público a quien va dirigido. Esta cuestión es muy amplia y, como es frecuente, no puede constreñirse a unas meras indicaciones, pues de cada experiencia pueden surgir, y de hecho así lo hemos experimentado, múltiples indagaciones y posibles razonamientos, cuando se llevan a la práctica. En este apartado, solo a título informativo, para posible inspiración de otros colegas, y como muestra de cómo se podría proceder, señalaremos algunas ideas al respecto.
En cuanto a conceptos, como se indicaba en la introducción, en el conjunto de experiencias se abordan una gran variedad de aspectos de física y de química, según se ha ido detallando.
Como ejemplos de cómo se puede promover la indagación, cualquiera de las experiencias podría ser muy enriquecedora al respecto. Por ejemplo, al abordar la primera de ellas (con CO2 sólido), se incidió en aspectos como la formación en algún caso (dependiendo de la cantidad de hielo seco añadido) de hielo (agua sólida) por el descenso de la temperatura por debajo de 0 ºC. Este hielo formado asciende por su menor densidad. También se comentó la formación de agua condensada en la pared externa del recipiente y se incluyó una referencia reciente donde se profundiza aún más en el razonamiento crítico de los fenómenos asociados. Otro fenómeno que se produce a veces es que el bloque de hielo seco, sobre ciertas superficies, vibra y se mueve emitiendo un zumbido característico.
Otros razonamientos se pueden asociar a la experiencia de la nieve artificial. Para niños pequeños se puede orientar como una experiencia espectacular, de la que, con las explicaciones pertinentes, se puede introducir el campo de nuevos materiales. Pero con estudiantes de mayor nivel educativo, se pueden hacer medidas con balanza para comprobar la conservación de la masa, tanto en la disolución del azúcar como en la preparación de nieve artificial. También se puede discutir, con esta misma experiencia, si el enfriamiento que se produce en la nieve artificial formada (apreciable al tacto) se debe a la evaporación del agua o a que el propio fenómeno de formación pudiera ser endotérmico.
Como ya se ha indicado, las actividades expuestas se han llevado a la práctica en varios entornos:
- Educativos formales. A lo largo del curso académico, se muestran algunas de las experiencias descritas para alumnos de Educación Secundaria Obligatoria, de bachillerato y universitarios de primer curso, en función de los contenidos abordados en el curso, la oportunidad y la disponibilidad de tiempo.
- Divulgativos. En talleres de dos tipos: grupos de alumnos que asisten con su profesor a otro centro educativo (por ejemplo durante la Semana de la Ciencia de Madrid), y talleres en ferias científicas donde se exponen al público asistente que va pasando (y que debe elegir entre otras propuestas divulgativas que se ofrecen simultáneamente).
En ambos, la respuesta apreciada en los distintos colectivos implicados ha sido altamente positiva. Para los docentes que preparan la actividad, supone un aprendizaje continuo de nuevas experiencias prácticas, pero también es un reto para la creatividad ante la necesidad de organizar una actividad tanto lúdica como formativa, adaptable a distintos entornos.
Por la acogida que tuvo el estand en el certamen de Ciencia en Acción y demás eventos en los que se ha realizado, se puede concluir que los participantes en la actividad suelen descubrir aplicaciones interesantes de la ciencia y aprecian el esfuerzo realizado. Aparte de aclarar algunas cuestiones y sorprenderse con efectos curiosos, adquieren o refuerzan la idea de que la ciencia en general, y la química en particular, es un ámbito de interés y esencial en la sociedad moderna.
Relacionado con el mundo del cine, se pretende que al final de la actividad, estudiantes y público tengan un interés hacia otras actividades de divulgación científica de tipo …to be continued más que de The end.
Este tipo de actividades es especialmente motivador también para alumnos colaboradores. Mientras explican todos estos experimentos que han preparado con cuidado, ellos mismos refuerzan sus conocimientos y les surgen interrogantes. En la figura 12 se ilustra cómo en un reciente festival de divulgación científica se instaló una mesa con los materiales para hacer los experimentos, con carteles explicativos al fondo, y el concurso de tres colaboradores que eran estudiantes universitarios y antiguos alumnos de educación secundaria de la profesora Prolongo. Tuvieron que explicar a público variado (niños de colegios, familias, ancianos…) algunas experiencias que habían estudiado en su instituto con la profesora unos años antes.

Figura 12.
Dos de los autores (M. L. Prolongo y G. Pinto) con los alumnos colaboradores S. Campos, M. A. Lozano y J.D. Diego, durante la presentación de las actividades en Algeciras (Cádiz), en octubre de 2016.
Por todo lo anterior, y en un contexto de generalización de oportunidades para la divulgación científica (Pinto 2003, Pinto et al. 2014), se recomienda la involucración de profesores e investigadores en ello, a través de distintas actividades y eventos.
Para citar este artículo: Pinto G., Prolongo
M. L., Alonso J. V. (2017) Química y física de algunos efectos especiales en cinematografía:
Una propuesta educativa y para la divulgación. Revista Eureka sobre
Enseñanza y Divulgación de las Ciencias 14 (2), 427-441. Recuperado de http://hdl.handle.net/10498/19227
http://revistas.uca.es/index.php/eureka/article/view/3160 (html)
Parte del trabajo preparatorio se realizó en el I.E.S. Manuel Romero (Villanueva de la Concepción, Málaga). Se agradece la colaboración de Soledad Campos, Miguel Ángel Lozano y Juan Diego Paradas, antiguos alumnos de este instituto (actualmente alumnos universitarios). Se agradece también la ayuda prestada por Francisco Díaz en la realización de fotografías, así como el apoyo recibido por la Universidad Politécnica de Madrid (proyecto de innovación educativa «Fomento del aprendizaje experiencial de la química»), la Fundación LaCaixa (proyecto «Ciencia y tecnología para todo y para todos»), y el programa Ciencia en Acción, que concedió a la actividad una mención de honor en el certamen celebrado en Algeciras (Cádiz) en 2016. Además, los autores desean expresar su gratitud por el trabajo realizado por los evaluadores del manuscrito.

Figura 1.
Cartel de una película cuyo título resume el mensaje principal que se pretende transmitir con las actividades propuestas y otras análogas.

Figura 2.
Resultado de la experiencia de añadir hielo sexo en disolución acuosa ligeramente básica con unas gotas de indicador azul de bromotimol, del que se incluye su estructura molecular (en función del pH).

Figura 3.
Cambio de color producido al enfriarse un envase termocrómico, inicialmente rosa a unos 22 ºC, y en una pajita (también termocrómica) que al principio era blanca, al estar en contacto con agua sobre la que se añadió hielo seco. En el caso de la pajita, se debe sorber el agua con aspirador manual para pipetas, para evitar riesgos.

Figura 4.
Ilustración del experimento propuesto para mostrar la formación de nieve artificial (explicación detallada en el texto), mediante un truco de magia, y la estructura del poliacrilato de sodio.

Figura 5.
Preparación de sangre artificial y estructura del complejo formado. Para evitar el contacto con la piel, se dispuso una capa de plástico invisible sobre la mano al realizar la fotografía.

Figura 6.
Ilustración de la reacción redox que produce el efecto de un «genio» saliendo de una botella. Aunque la profesora que realizó el proceso no lleva protección en los ojos, se debe a que la fotografía se tomó extremando las precauciones. Debe procederse siempre con gafas de seguridad.

Figura 7.
Maqueta de volcán realizada por uno de los autores (J.V.A.) y «erupción» provocada por la reacción redox discutida en el texto. Esta experiencia se lleva a cabo en vitrina de gases de laboratorio.

Figura 8.
Cristales preparados por alumnos del I.E.S. Manuel Romero (Villanueva de la Concepción, Málaga) y comparación con la kryptonita de Supermán.

Figura 9.
Aspecto del bote con la esfera de poliacrilato de sodio hidratado (indistinguible si está sumergida en agua) y niños observando con asombro cómo aparece la bola al retirar el agua.

Figura 10.
Materiales necesarios para preparar un tipo de tinta invisible y para provocar su visibilidad.

Figura 11.
Ilustración de la fabricación de cerveza artificial según el proceso redox explicado en el texto.

Figura 12.
Dos de los autores (M. L. Prolongo y G. Pinto) con los alumnos colaboradores S. Campos, M. A. Lozano y J.D. Diego, durante la presentación de las actividades en Algeciras (Cádiz), en octubre de 2016.
